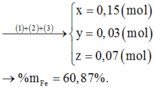Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pu tạo kết tủa BaCO3 và CaCO3
Ta thấy :khi thế 2 nguyên tử Cl bằng 1 nhóm CO3, khối lượng dung dịch giảm 35,5*2-60=11g
Mà khối lượng theo đầu bài giảm 43-39,7=3,3g>>n(BaCO3 và CaCO3)=3,3/11=0,3mol
Đặt nBaCO3=a;nCaCO3=B
>>Ta có hệ :197a+100b=39,7 và a+b=0,3>>a=0,1;b=0,2
>>%m BaCO3 =19,7/39,7*100=49,62%>>%CaCO3=50,38%

Đáp án B
Phương pháp:
Bảo toàn electron
Bảo toàn điện tích
Bảo toàn nguyên tố Fe, O, H
Hướng dẫn giải:
Phần kết tủa có nAgCl= 0,3 => nAg = 0,009
Bảo toàn electron: nFe2+ = nAg + 3nNO = 0,036
nNO = 0,009 => nH+ dư = 4nNO = 0,036
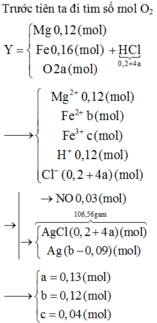
Đặt a, b, c là số mol Fe, Fe3O4, Fe(NO3)2 trong X
=> mX = 56a + 232b + 180c = 7,488 (1 )
Dung dịch Y còn H+ dư và Fe2+ nên NO3- đã hết.
Vậy Y chứa Fe2+ (0,036), H+ (0,036), Cl- (0,3)
Bảo toàn điện tích => nFe3+ = 0,064
Bảo toàn Fe => a + 3b + c = 0,064 + 0,036 (2)
Bảo toàn H => nH2O = 0,144
Bảo toàn O:
4nFe3O4 + 6nFe(NO3)2 + 3nHNO3 = nZ + nH2O
=> 4b + 6c + 0,024 . 3 = 0,032 + 0,144 (3)
Giải hệ (1)(2)(3): a = 0,05 b = 0,014 c = 0,008
=> %Fe = 37,4%

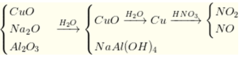
Ta có: n N a 2 O = n A l 2 O 3 = 0 , 4 . 0 , 5 2 = 0 , 1

⇒ n C u = 0 , 005 + 0 , 015 . 3 2 = 0 , 025 ⇒ m = 0 , 025 . 80 + 0 , 1 . 62 + 0 , 1 . 102 = 18 , 4 Đ á p á n C

Ta có: \(n_{NH_3}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
\(n_{AlCl_3}=0,1.1=0,1\left(mol\right)\)
PT: \(3NH_3+AlCl_3+3H_2O\rightarrow Al\left(OH\right)_3+3NH_4Cl\)
Xét tỉ lệ: \(\dfrac{0,3}{3}=\dfrac{0,1}{1}\), ta được pư vừa đủ.
⇒ nAl(OH)3 = 0,1 (mol)
⇒ mAl(OH)3 = 0,1.78 = 7,8 (g)
Pt ion : \(NH_4+OH^--->NH_3+H_2O\)
Do đó chất khi thu được là NH3 --> \(n_{NH3}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
Ta có : \(n_{AlCl3}=0,1.1=0,1\left(mol\right)\)
\(AlCl_3+3NH_3+H_2O\rightarrow Al\left(OH\right)_3+3NH_4Cl\)
0,1 0,3 0,1
Xét tỉ lệ :\(\dfrac{0,1}{1}=\dfrac{0,3}{3}\Rightarrow phản.ứng.hết\)
\(\Rightarrow m_{kt}=0,1.78=7,8\left(g\right)\)