Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

a) \(PTHH:2Al+6HCl\xrightarrow[]{}2AlCl_3+3H_2\)
b) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{Al}=\dfrac{0,15.2}{3}=0,1\left(mol\right)\)
\(m_{Al}=0,1.27=2,7\left(g\right)\)
c)\(n_{AlCl_3}=\dfrac{0,15.2}{3}=0,1\left(mol\right)\)
\(m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\)

n H2=\(\dfrac{8,96}{22,4}\)=0,4 mol
2Al + 6HCl→2AlCl3 + 3H2 (1)
x----------------------------3\2x
Zn +2 HCl→ZnCl2 + H2 (2)
y----------------------------y mol
ta có hệ :
27x+65y=11,9
\(\dfrac{3}{2}\)x+y=0,4
=>x=0,2 mol->m Al=0,2.27=5,4g
=>y=0,1 mol->m Zn=0,1.65=6,5g
nắm chắc pthh là xong hết , về luyện là đc
\(nH_2=8,96:22,4=0,4mol\)
PTHH:
\(2Al+2Zn+2HCl\rightarrow2AlZnCl+H_2\)
0,8<--0,8<----0,8<------<0,8--------<0,4
\(mAl=0,8.27=21,6gam\)
\(mZn=0,8.65=52gam\)
\(mAlZnCl=102gam\)

\(PTHH:Zn+2HCl->ZnCl_2+H_2\)
ap dung DLBTKL ta co
\(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\)
\(=>m_{H_2}=m_{Zn}+m_{HCl}-m_{ZnCl_2}\\ =>m_{H_2}=13+14,6-27,2\\ =>m_{H_2}=0,4\left(g\right)\)

bài này quá dễ nha.Em dùng bảo toàn khối lượng là ra ngay nà
mZn + mHCl = mZnCl2 + mH2
=>mHCl =(mZnCl2 + mH2) - mZn
= (340+5) -162.5= 182.5g
vậy khối lượng HCl phản ứng là 182.5g
Chúc em học tốt !!!!:))

Nzn=0,1mol
a) có pt : Zn + 2Hcl -> ZnCl2 + H2
1 -> 2 -> 1 -> 1 mol
0,1-> 0,2 -> 0,1 -> o,1 mol
b) số Hcl đã dùng khi pứ là :
0,2 . 36,5= 7,3
-> số gam hcl dư là 10,95- 7,3=3,65(g)
c)mZnCl2=0,1 . 136=13,6g
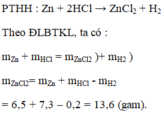
2Al+6HCl--->2AlCl3+3H2
x------3x
Zn+2HCl--->ZnCl2+H2
y-------2y
Ta có
n HCl=36,5/36,5=1(mol)
Theo bài ta có hệ pt
\(\left\{{}\begin{matrix}27x+65y=18,4\\3x+2y=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
mAl=0,2.27=5,4(g)
mZn=0,2.65=13(g)