Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

4P + 5 O2 -to-> 2 P2O5
P2O5 +3 H2O -> 2 H3PO4
H3PO4 là axit trung bình (sau này em sẽ học) -> Qùy tím hóa đỏ
Chúc em học tốt!

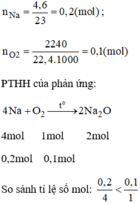
Vậy O 2 dư.
Sau phản ứng Na không dư nên không có khí H 2 bay ra, quỳ tím chuyển sang màu xanh vì:
N a 2 O + H 2 O → 2 N a O H

a.\(2Na+2H_2O\rightarrow2NaOH+H_2\)
-> phenol phtalein chuyển sang màu hồng nhạt
b.\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(SO_2+H_2O\rightarrow H_2SO_3\)
-> quỳ tím hóa đỏ
c.\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
d.\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
e.\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
f.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
-> que đóm bùng cháy sáng
Bổ sung thêm cho Nguyễn Ngọc Yến Trang :)
c) Phản ứng cháy sáng, không lửa, không khói tạo ra các hạt nóng chảy màu nâu
d) Chất rắn màu đen CuO chuyển dần sang màu đỏ (Cu) và xung quanh thành ống nghiệm có xuất hiện những giọt nước nhỏ
e) Zn tan dần, có sủi bọt khí không màu, mùi

\(n_{Na}=\dfrac{18,4}{23}=0,575\left(mol\right)\\
n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\
pthh:4Na+O_2\underrightarrow{t^o}2Na_2O\)
0,575 0,2875
\(m_{Na_2O}=62.0,2875=17,825g\)
\(pthh:Na_2O+H_2O\rightarrow2NaOH\)
Na2O tan ra tạo thành dd NaOH
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\
pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48l\\
m_{FeSO_4}=127.0,2=25,4g\)
FeSO4 - sắt (II) sunfat - muối trung hòa
\(pthh:Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
0,2 0,15
\(m_{Fe}=0,15.56=8,4g\)

Nêu và giải thích hiện tượng xảy ra trong các thí nghiệm sau, viết PTHH
a) Đốt dây sắt quấn hình lò xo trong lọ đựng khí O2
Dây sắt cháy mạnh trong khí oxi, sáng chói, không có ngọn lửa, không có khói, tạo ra các hạt nhỏ nóng chảy màu nâu là sắt ( II, III) oxit, công thức hóa học là Fe3O4, còn gọi là oxit sắt từ.
PTHH : 3Fe +2O2--to⟶Fe3O4
b) Cho viên kẽm vào ống nghiệm đựng dd HCL
Hiện tượng khi cho viên kẽm (Zn) vào dung dịch axit clohiđric (HCl) là : viên kẽm tan dần, có khí không màu thoát ra.
Giải thích: Do Zn tác dụng với dd HCl
PTHH: Zn + 2HCl → ZnCl2 + H2
Theo thời gian kẽm sẽ bị ăn mòn chậm dần do nồng độ của HCl giảm dần
c) Dẫn luồng khí H2 đi qua bột CuO nung nóng
Khi đốt nóng tới khoảng 400 độ C: Bột CuO màu đen chuyển dần thành lớp đồng kim loại màu đỏ gạch và có hơi nước đọng ở thành ống nghiệm
PTHH:CuO+H2-to-->Cu+H2O
d) cho mẩu NA vào cốc đựng H2O có sẵn mẩu quỳ tím
Hiện tượng: kim loại Na tan trong nước, phản ứng mãnh liệt, tỏa nhiều nhiệt và sủi bọt khí không màu là H2. Mẫu giấy quỳ tím chuyển dần sang màu xanh.
Giải thích:
Do Na tác dụng với H2O
PTHH: 2Na +2H2O -> 2NaOH + H2
NaOH là bazo nên làm qùy tím hóa xanh.

1) S+O2->SO2
SO2+H2O->H2SO3(axit)
-> làm quỳ tím đổi màu hồng đỏ vì chất thu được là axit
2)2NA+2H2O->2NAOH(bazo)+H2
->làm quỳ tím đổi màu xanh vì dung dịch thu được là bazo
3)MgO+H2O->Mg(OH)2(bazo)
->làm quỳ tím chuyển thành màu xanh vì chất thu được là bazo

a. H.tượng: Cháy với ngọn lửa xanh nhạt và có thể gây nổ nếu đúng với tỉ lệ \(\dfrac{n_{H_2}}{n_{O_2}}=\dfrac{2}{1}\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
b. H.tượng: Tạo ra khí có mùi hắc
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
c. H.tượng: P cháy mãnh liệt, cho nước vào tạo thành dd và quỳ tím sẽ chuyển sang màu đỏ
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
d.H.tượng: Sắt cháy mạnh, không có ngọn lửa, không có khói, tạo thành oxit sắt từ
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
e. H.tượng: Na tan dần, sủi bọt khí, dd dần chuyển sang màu hông
\(2Na+2H_2O\rightarrow2NaOH+H_2\uparrow\)
g. H.tượng: CaO tan một phần, quỳ tím dần chuyển sang màu xanh
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Bổ sung nội dung còn thiếu
a) ko cần đúng tỉ lệ , H2, khi gặp O2 khi đốt vẫn có nổ nhỏ
c) Tạo ra khói trắng , sau đó cho nước , phần chất bột trắng tan
d) Ko phải là ko có ngọn lửa , đây ngọn lửa cháy sáng
e) Na vừa tan , vừa chạy trên mặt nước
g) CaO tan ít , tạo nhũ trắng