Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học:
a) H2 (k) + Cl2 (k) → 2HCl(k) (HCl ở trạng thái khí, không màu)
b) S + H2 (k) → H2S (k) (H2S ở trạng thái khí, không màu, có mùi trứng thối)
c) H2 + Br2 → 2HBr(to) (HBr ở trạng thái khí, không màu)

a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

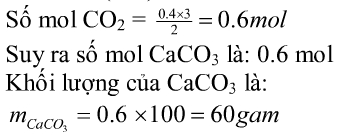
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g

Các phương trình hóa học:
a) С + 2CuO 2Cu + CO2
b) С + 2PbO 2Pb + CO2
c) С + CO2 2CO
d) С + 2FeO 2Fe + CO2
Các phản ứng trên dều thuộc loại phản ứng oxi hóa - khử. Vai trò của с là chất khử. Các phản ứng:
a), b) dùng điều chế kim loại.
c), d) xảy ra trong quá trình luyện gang, dùng luyện gang.

(a) Gọi CTPT của các chất là CxHyOz
M<170 => mC<170.55,8% => 12x<94,86 => x<7,9
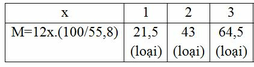
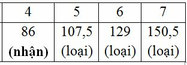
Vậy CTPT có dạng: C4HyOz (y≤10)(Do M là các số nguyên và là số chẵn)
Ta có: 12.4 + y + 16z = 86 => y + 16z = 38
+ z = 1: y = 22 (loại)
+ z = 2: y = 6 (nhận)
Vậy CTPT của các chất là: C4H6O2
b) A, B đều có nhóm CH3 và phản ứng với NaHCO3 tạo khí và chỉ có B có đồng phân hình học nên cấu tạo của A và B là:
A: CH2=C(CH3)-COOH
B: CH3-CH=CH-COOH
F, H, K có phản ứng với NaHCO3 tạo khí nên F, H, K là các axit.
- G là hợp chất không bền và chuyển hóa ngay thành G’ (G và G’ có cùng công thức phân tử) và khi oxy hóa bằng H2CrO4, hợp chất G’ chuyển hóa thành F nên G’ và F có cùng số nguyên tử C
C: CH3COOCH=CH2
F: CH3COOH
G: CH2=CH-OH
G’: CH3CHO
- H có phản ứng với NaHCO3 tạo khí nên H là axit. Mặt khác, phản ứng của H với bạc nitrat trong amoniac chỉ tạo thành các chất vô cơ nên H là HCOOH
D: HCOOCH2-CH=CH2
H: HCOOH
I: CH2=CH-CH2-OH
- L bị oxi hóa tạo HCOOH nên L là CH3OH
E: CH2=CH-COOCH3
K: CH2=CH-COOH
L: CH3OH
(1) CH2=C(CH3)-COOH (A) + NaHCO3 → CH2=C(CH3)-COONa + H2O + CO2
(2) CH3-CH=CH-COOH (B) + NaHCO3 → CH3-CH=CH-COONa + H2O + CO2
(3) CH3COOCH=CH2 (C) + NaOH → CH3COONa + CH3CHO (G’)
(4) CH3COONa + HCl → CH3COOH (F) + NaCl
(5) HCOOCH2-CH=CH2 (D) + NaOH → HCOONa + CH2=CH-CH2-OH (I)
(6) HCOONa + HCl → HCOOH (H) + NaCl
(7) CH2=CH-COOCH3 (E) + NaOH → CH2=CH-COONa + CH3OH (L)
(8) CH2=CH-COONa + HCl → CH2=CH-COOH (K) + NaCl
(9) CH3CHO + H2CrO4 → CH3COOH + H2CrO3
(10) CH3OH + 2H2CrO4 → HCOOH + 2H2CrO3 + H2O
(11) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag + 2NH4NO3
(c) Phản ứng polime hóa của A và C:
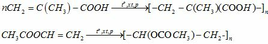
(d)


\(n_{MgCO3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
a) Pt : \(2CH_3COOH+MgCO_3\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O|\)
2 1 1 1 1
0,2 0,1 0,1 0,1
b) \(n_{CH3COOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{CH3COOH}=0,2.60=12\left(g\right)\)
\(C_{ddCH3COOH}=\dfrac{12.100}{200}=6\)0/0
\(n_{\left(CH3COO\right)2Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{\left(CH3COO\right)2Mg}=0,1.142=14,2\left(g\right)\)
\(m_{ddspu}=8,4+200-\left(0,1.44\right)=204\left(g\right)\)
\(C_{dd\left(CH3COO\right)2Mg}=\dfrac{14,2.100}{204}=6,96\)0/0
Chúc bạn học tốt

a) 2CO + O2 2CO2
Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép.
b) CO + CuO CO2 + Cu
Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao.
Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu.
a) 2CO + O2 2CO2
Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép.
b) CO + CuO CO2 + Cu
Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao.
Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu.

nA = = 0,015625 mol.
MA = = 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x = 32g => nO =
= 2 mol
mS = 64 - 32 = 32g => ns = = 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
b) Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối:
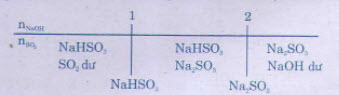
Bài 7*. a) Hãy xác định công thức của hợp chất khí A, biết rằng :
- A là oxit của lưu huỳnh chứa 50% oxi.
- 1 gam khí A chiếm thề tích là 0,35 lít ở đktc.
b) Hoà tan 12,8 gam hợp chất khí A vào 300 ml dung dịch NaOH 1,2M. Hãy cho biết muối nào thu được sau phản ứng. Tính nồng độ mol của muối (giả thiết thể tích dung dịch thay đổi không đáng kể).
Lời giải:
nA = = 0,015625 mol.
MA = = 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x = 32g => nO =
= 2 mol
mS = 64 - 32 = 32g => ns = = 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
b) * Hướng dẫn: Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối:


Số hiệu là 11
Cấu tạo nguyên tử: Na
Tính chất hóa học đặc trưng là kim loại hoạt động mạnh
Tính chất hóa học của A mạnh hơn Mg, Al
ài 4. Nguyên tố A có số hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng tuần hoàn các nguyên tố hoá học. Hãy cho biết:
- Cấu tạo nguyên tử của A.
- Tính chất hoá học đặc trưng của A.
- So sánh tính chất hoá học của A với các nguyên tố lân cận.
giải
Số hiệu là 11
Cấu tạo nguyên tử: Na
Tính chất hóa học đặc trưng là kim loại hoạt động mạnh
Tính chất hóa học của A mạnh hơn Mg, Al
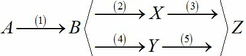
a)
CnH2n+2 + (1,5n + 0,5)O2 → nCO2 + (n + 1)H2O
1 → 1,5n + 0,5 n n + 1
Theo đề bài: nkhí trước pứ = nkhí sau pứ → 1 + 1,5n + 0,5 = n + n + 1 → n = 1
→ A: CH4
b)
R là chất dẻo nên R có thể là: PE, PVC, PA, PS → X có chứa liên kết đôi