
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



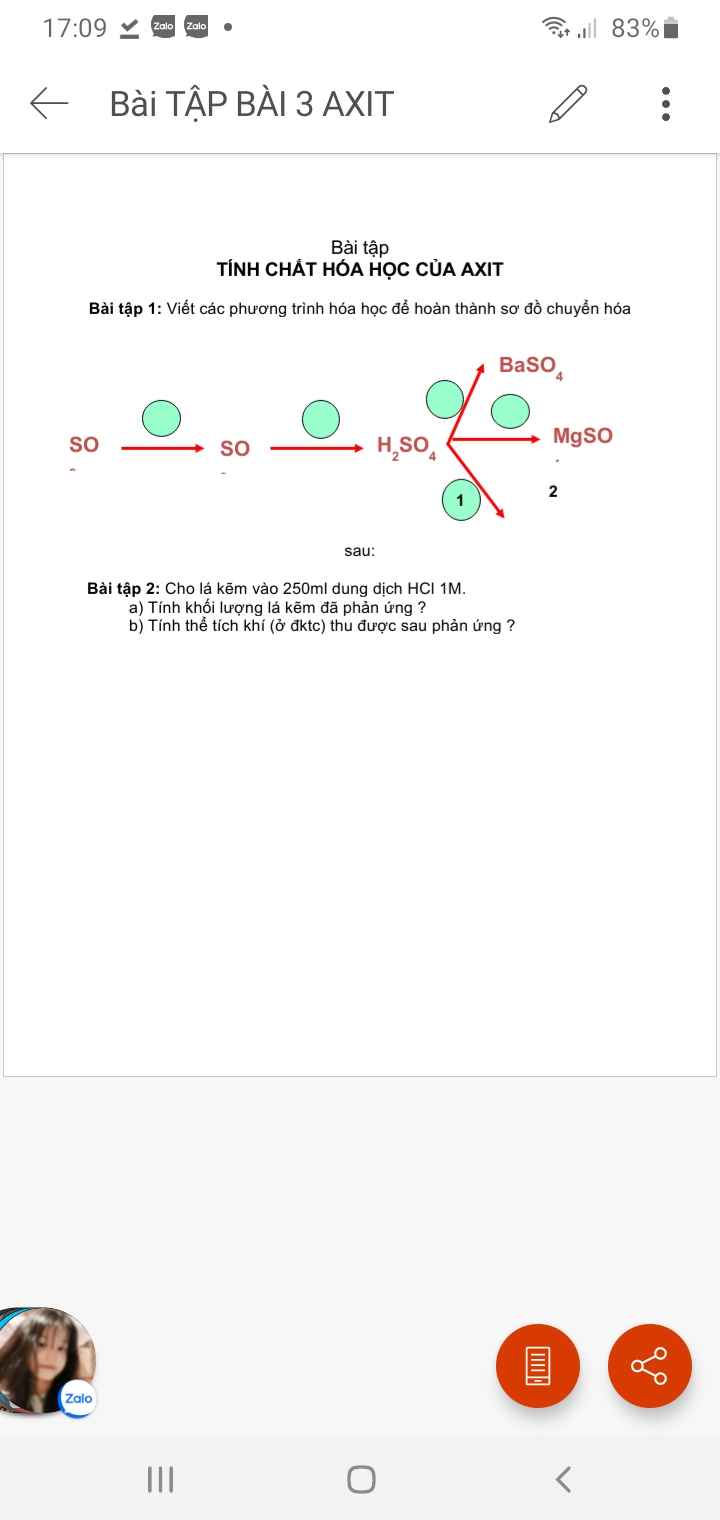
\(a,\left(1\right)2Fe\left(OH\right)_3\underrightarrow{^{to}}Fe_2O_3+3H_2O\\ \left(2\right)Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \left(3\right)Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow3BaSO_4\downarrow+2FeCl_3\\ \left(4\right)FeCl_3+3KOH\rightarrow Fe\left(OH\right)_3+3KCl\)
\(b,\left(1\right)CaCO_3\underrightarrow{^{to}}CaO+CO_2\\ \left(2\right)CaO+2HCl\rightarrow CaCl_2+H_2O\\ \left(3\right)CaCl_2+2AgNO_3\rightarrow2AgCl\downarrow+Ca\left(NO_3\right)_2\\ \left(4\right)Ca\left(NO_3\right)_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaNO_3\\ \left(5\right)CaCO_3+2HNO_3\rightarrow Ca\left(NO_3\right)_2+CO_2+H_2O\)

\((1)2Al+6HCl\to 2AlCl_3+3H_2\\ (2)AlCl_3+3AgNO_3\to Al(OH)_3\downarrow+3AgCl\\ (3)2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ (4)2Al_2O_3\xrightarrow{đpnc}4Al+3O_2\)

Gọi kim loại là R, hóa trị n, do R là kim loại nên n có thể bằng 1, 2 hoặc 3
\(2R + 2nHCl \rightarrow 2RCl_n + nH_2\)
\(n_{H_2}=\dfrac{3,36}{22,4}= 0,15 mol\)
Theo PTHH:
\(n_{R}= \dfrac{2}{n} . n_{H_2}= \dfrac{2}{n} . 0,15 = \dfrac{0,3}{n} mol\)
\(\Rightarrow M_R= \dfrac{3,6}{\dfrac{0,3}{n}}=\dfrac{3,6n}{0,3}=12n\)
Do n bằng 1, 2 hoặc 3
Ta thấy n= 2 và MR= 24 g/mol thỏa mãn
R là Mg
Gọi CTHH của kim loại là M, x là hóa trị của M
PTHH: M + xHCl ---> MClx + \(\dfrac{x}{2}\)H2.
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_M=\dfrac{1}{\dfrac{x}{2}}.n_{H_2}=\dfrac{1}{\dfrac{x}{2}}.0,15=\dfrac{2}{x}.0,15=\dfrac{0,3}{x}\left(mol\right)\)
=> \(M_M=\dfrac{3,6}{\dfrac{0,3}{x}}=\dfrac{3,6x}{0,3}=12x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 | 4 |
| M | 12 | 24 | 36 | 48 |
| Loại | (TM) | loại | Loại |
Vậy MM = 24(g)
Dự vào bảng hóa trị, suy ra:
M là magie (Mg)


Bài 4 :
100ml = 0,1l
300ml = 0,3l
\(n_{Na2SO4}=0,2.0,1=0,02\left(mol\right)\)
\(n_{BaCl2}=0,1.0,3=0,03\left(mol\right)\)
Pt : \(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4|\)
1 1 2 1
0,02 0,03 0,04 0,02
a) Lập tỉ số so sánh : \(\dfrac{0,02}{1}< \dfrac{0,03}{1}\)
⇒ Na2SO4 phản ứng hết , BaCl2 dư
⇒ Tính toán dựa vào số mol của Na2SO4
\(n_{BaSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{BaSO4}=0,02.233=4,66\left(g\right)\)
b) \(n_{NaCl}=\dfrac{0,02.2}{1}=0,04\left(mol\right)\)
\(n_{BaCl2\left(dư\right)}=0,03-0,02=0,01\left(mol\right)\)
\(V_{ddspu}=0,1+0,3=0,4\left(l\right)\)
\(C_{M_{NaCl}}=\dfrac{0,04}{0,4}=0,1\left(M\right)\)
\(C_{M_{BaCl2\left(dư\right)}}=\dfrac{0,01}{0,4}=0,025\left(M\right)\)
Chúc bạn học tốt

Câu 4:
a) nC2H6O=0,3(mol)
PTHH: C2H6O + 3 O2 -to-> 2 CO2 + 3 H2O
0,3___________0,9_____0,6(mol)
=>V(CO2,đktc)=0,6 x 22,4= 13,44(l)
b) V(kk,dktc)=V(O2,dktc) . 100/20 = (0,9.22,4).5=100,8(l)
Câu 5:
C2H6O + 3 O2 -to-> 2 CO2 + 3 H2O
nH2O=0,9(mol)
=> nCO2= 2/3. 0,9=0,6(mol)
a) V(CO2,đktc)=0,6.22,4=13,44(l)
b) Vkk=5.V(O2,dktc)= 5.(0,9.22,4)= 100,8(l)

Bài 2:
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2O\)
Ta có: \(n_{Zn}=n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}\cdot0,25=0,125\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,125\cdot65=8,125\left(g\right)\\V_{H_2}=0,125\cdot22,4=2,8\left(g\right)\end{matrix}\right.\)





giải giúp bạn bài nào?
cho các dd sau:H2S04,CuSO4,BA(OH)2,NaOH,HCL lần lượt phản ứng với nhau từng đôi một.Viết pt hoá học xảy ra(nếu có)