Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy đổi hh thành Fe và O
Đặt nFe=a(mol);nO=b(mol); nSo2=c(mol).
=> \(56a+16b=69.6\)(1)
Bảo toàn e => \(3a-2b-2c=0\)(2)
Kết tủa Fe(OH)3: \(n_{Fe\left(OH\right)_3}=0.7\left(mol\right)\)
=> \(n_{H^+_{\left(du\right)}}=1,55.2-0,7.3=1\left(mol\right)\)
=> \(n_{H_2SO_4\left(pu\right)}=2-0,5=1,5\left(mol\right)\)
=> \(b+2c=1,5\) (3)
Từ (1)(2) (3)
=> \(\left\{{}\begin{matrix}a=0,9\left(mol\right)\\b=1,2\left(mol\right)\\c=0,15\left(mol\right)\end{matrix}\right.\)=> \(V=3,36\left(l\right)\)
Quy đổi hỗn hợp ban đầu về a mol Fe; b mol O.
\(\Rightarrow56a+16b=69,6\left(1\right)\)
TN1: Cho hỗn hợp td H2SO4
\(n_{H_2SO_4}=2\left(mol\right)\)
QT nhường e: Fe -----> Fe+3 + 3e
____________a\(_{\rightarrow}\)______________3a
QT nhận e: O + 2e ------> O-2
__________b\(_{\rightarrow}\)__2b
S+6 + 2e -----> S+4
______3a+2b____\(_{\leftarrow}\frac{3a+2b}{2}\)
TN2: Cho Y td NaOH
Sau pứ ta có Fe(OH)3 ; Fe2(SO4)3(dư); Na2SO4
\(n_{NaOH}=3,1\left(mol\right);n_{Fe\left(OH\right)_3}=0,7\left(mol\right)\\ BTNT.Na\Rightarrow n_{Na_2SO_4}=\frac{1}{2}n_{NaOH}=1,55\left(mol\right)\\ BTNT.Fe\Rightarrow n_{Fe}=2n_{Fe_2\left(SO_4\right)_3\left(du\right)}+n_{Fe\left(OH\right)_3}\\ \Rightarrow n_{Fe_2\left(SO_4\right)_3\left(du\right)}=\frac{a-0,7}{2}\left(mol\right)\\ \\ BTNT.S\Rightarrow n_{H_2SO_4}=3n_{Fe_2\left(SO_4\right)_3\left(du\right)}+n_{SO_2}+n_{Na_2SO_4}\\ \Rightarrow2=1,5\left(a-0,7\right)+\frac{3a-2b}{2}+1,55\left(2\right)\)
(1) và (2) => \(\left\{{}\begin{matrix}a=0,9\\b=1,2\end{matrix}\right.\)
\(\Rightarrow n_{SO_2}=0,15\left(mol\right)\Rightarrow V=3,36\left(l\right)\)

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng. Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
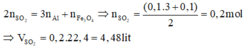

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng.Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
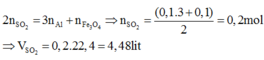

a)
n KMnO4 = 0,26(mol)
Bảo toàn electron :
5n KMnO4 = 2n SO2
<=> n SO2 = 0,26.5/2 = 0,65(mol)
V SO2 = 0,65.22,4 = 14,56 lít
b)
n H2SO4 pư = 2n SO2 = 0,65.2 = 1,3(mol)
n H2SO4 dư = 1,3.10% = 0,13(mol)
=> n H2SO4 đã dùng = 1,3 + 0,13 = 1,43(mol)
C% H2SO4 = 1,43.98/150 .100% = 93,43%

Coi hh gồm Fe và O.
Ta có: 56nFe + 16nO = 14,64 (1)
Ta có: \(n_{NO}=\dfrac{1,4874}{24,79}=0,06\left(mol\right)\)
Theo ĐLBT e, có: 3nFe = 2nO + 3nNO ⇒ 3nFe - 2nO = 0,06.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,201\left(mol\right)\\n_O=0,2115\left(mol\right)\end{matrix}\right.\)
⇒ m = mFe = 0,201.56 = 11,256 (g)

a, \(Fe+H_2SO_{4\text{loãng}}\rightarrow FeSO_4+H_2\)
\(n_{Fe}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(Fe+H_2SO_{4\text{đặc}}\rightarrow Fe_2\left(SO_4\right)_3+SO_2+H_2O\)
\(Cu+H_2SO_{4\text{đặc}}\rightarrow CuSO_4+SO_2+H_2O\)
Bảo toàn e:
\(2n_{Cu}+3n_{Fe}=2n_{SO_2}\)
\(\Leftrightarrow n_{Cu}=\dfrac{2n_{SO_2}-3n_{Fe}}{2}=0,25\left(mol\right)\)
\(\Rightarrow x=m_{Cu}+m_{Fe}=0,25.64+0,5.56=44\left(g\right)\)
a) Đặt \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)=b=n_{Fe}\\n_{SO_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\end{matrix}\right.\)
Bảo toàn electron: \(2a+3b=2\) \(\Rightarrow2a+3\cdot0,5=2\) \(\Rightarrow a=n_{Cu}=0,25\left(mol\right)\)
\(\Rightarrow x=m_{Cu}+m_{Fe}=0,25\cdot64+0,5\cdot56=44\left(g\right)\)
b) Ta có: \(n_{H_2SO_4\left(p/ư\right)}=\dfrac{1}{2}n_{e\left(traođổi\right)}+n_{SO_2}=\dfrac{1}{2}\cdot2+1=2\left(mol\right)\)
\(\Rightarrow\Sigma n_{H_2SO_4\left(đặc\right)}=2\cdot110\%=2,2\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{2,2\cdot98}{98\%}=220\left(g\right)\) \(\Rightarrow V_{H_2SO_4}=\dfrac{220}{1,84}\approx119,57\left(ml\right)\)
c) Ta có: \(\left\{{}\begin{matrix}n_{SO_2}=1\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,4\cdot1,5=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo 2 muối
PTHH: \(2SO_2+Ba\left(OH\right)_2\rightarrow Ba\left(HSO_3\right)_2\)
2x x x (mol)
\(SO_2+Ba\left(OH\right)_2\rightarrow BaSO_3\downarrow+H_2O\)
y y (mol)
Ta lập được hệ phương trình: \(\left\{{}\begin{matrix}x+y=0,6\\2x+y=1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=n_{Ba\left(HSO_3\right)_2}=0,4\left(mol\right)\\y=0,2\end{matrix}\right.\)
\(\Rightarrow C_{M_{Ba\left(HSO_3\right)_2}}=\dfrac{0,4}{0,4}=1\left(M\right)\)

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)