Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,NTDD:N\\ \%_N=\dfrac{28}{80}\cdot100\%=35\%\\ b,m_N=5\cdot35\%=1,75\left(kg\right)\)

a) Có 1 nguyên tố là P
b) Khối lượng mol của Ca3(PO4)2:
Mca3(po4)2= 3.40+2.15+2.4.8= 214 (g/mol)
Thành phần phần trăm của ng tố dinh dưỡng trong phân bón là:
%P=3.40.100/214= 56%

a, Có hai nguyên tố là K và N
Tên: kali nitrat
b, \(M_{KNO_3}=39+14+3.16=101\left(g/mol\right)\)
\(\%K=\dfrac{39.100}{101}=38,6\%;\%N=\dfrac{14.100}{101}=13,86\%\)

Chọn D
(1) Sai :(N H 4 ) 2 S O 4 chứa nguyên tố N nên dùng để cung cấp phân đạm cho cây, không chứa Photpho → không dùng để cung cấp phân lân
(2) Đúng: Phần trăm khối lượng N có trong phân hóa học là:
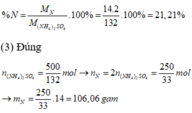
(4) Sai vì phân này tan hoàn toàn trong nước
(5) Sai vì phân ure (N H 2 ) 2 CO có hàm lượng N cao hơn phân (N H 4 ) 2 S O 4
→ thay ure bằng phân này sẽ giảm hàm lượng nguyên tố dinh dưỡng
→ ít lợi hơn
Vậy có 2 phát biểu đúng

Nguyên tố dinh dưỡng là N:
Ta có: \(n_{CO\left(NH_2\right)_2}=\dfrac{150}{60}=2,5\left(mol\right)\)
\(\Rightarrow m_{N_{\left(CO\left(NH_2\right)_2\right)}}=2,5.14.2=70\left(g\right)\)
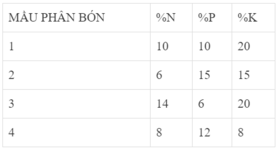
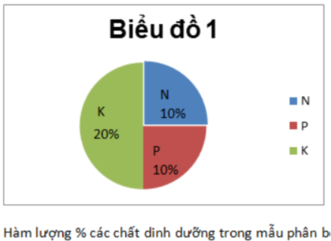
Coi $m_{phân\ ure} = 100(gam)$
$m_{CO(NH_2)_2} = 100.75\% = 75(gam)$
$n_{CO(NH_2)_2} = \dfrac{75}{60} = 1,25(mol)$
$n_N = 2n_{CO(NH_2)_2} = 1,25.2 = 2,5(mol)$
Phần trăm dinh dưỡng : $\%N = \dfrac{2,5.14}{100}.100\% = 35\%$