Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Rắn X phải có A1 dư vì chỉ có A1 mới phản ứng với dung dịch NaOH tạo khí H2. Mặt khác do phản ứng hoàn toàn nên Fe3O4 hết.
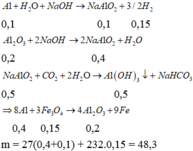

Đáp án B
Sau khi hỗn hợp X bị CO lấy
đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron:
3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3:
200a = 18 (2)
+ Giải hệ (1) và (2) ta có:
a = b = 0,09 mol
⇒ mY = 0,09(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi
= 6,48 + 0,04×16 = 7,12 gam

Kim loại không tan là Cu dư.
Cu dư => Muối thu được gồm FeCl2 và CuCl2 vì: Cu + 2FeCl3 → CuCl2 + 2FeCl2
Số mol các chất là: 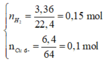
Sơ đồ phản ứng:
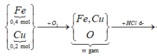
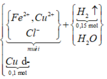
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Đáp án A.

HD: Gọi x, y tương ứng là số mol của Cu phản ứng và Cu dư sau phản ứng (1)
Cu + 2AgNO3 ---> Cu(NO3)2 + 2Ag (1)
x 2x x 2x
Dung dịch X gồm Cu(NO3)2 : 2x mol và AgNO3 dư: 2x mol. Chất rắn Y gồm Ag: 2x mol và Cu dư: y mol.
Zn + 2AgNO3 ---> Zn(NO3)2 + 2Ag (2)
0,05-x 0,1-2x 0,1-2x
Zn + Cu(NO3)2 ---> Zn(NO3)2 + Cu (3)
x x x
Số mol AgNO3 ban đầu = 0,2.0,5 = 0,1 mol; số mol Zn = 0,1 mol. Chất rắn Z gồm Cu (x mol), Ag (0,1-2x mol) và Zn (0,1-x-0,05+x) dư.
Ta có: 108(0,1-2x) + 64.x + 65.[0,1 - x - (0,05 - x)] = 7,97. Suy ra x = 0,04 mol.
Mặt khác, chất rắn Y có khối lượng: 64y + 2x.108 = 18,88 Suy ra y = 0,16 mol.
Như vậy, số mol của Cu ban đầu = x + y = 0,2 mol. Nên m = 64.0,2 = 12,8 g.
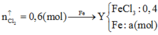
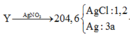

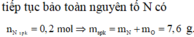

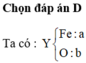
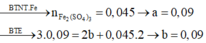
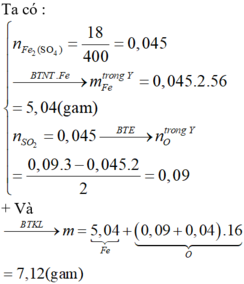
Câu 1/
\(2C\left(\dfrac{m}{12}\right)+O_2\left(\dfrac{m}{24}\right)\rightarrow2CO_2\left(\dfrac{m}{12}\right)\)
\(CO_2\left(\dfrac{m}{12}\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(\dfrac{m}{12}\right)+H_2O\)
Nếu như O2 thì tỷ khối của hỗn hợp so với O2 phải là: \(\dfrac{44}{32}=1,375>1,25\) vậy trong hỗn hợp khí phải có O2
\(n_C=\dfrac{m}{12}\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{V}{22,4}-\dfrac{m}{12}\left(mol\right)\)
\(\Rightarrow\dfrac{44.\dfrac{m}{12}+32.\left(\dfrac{V}{22,4}-\dfrac{m}{24}\right)}{\dfrac{m}{12}+\dfrac{V}{22,4}-\dfrac{m}{24}}=1,25.32=40\)
\(\Leftrightarrow15V-28m=0\left(1\right)\)
Ta lại có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(\Rightarrow\dfrac{m}{12}=0,06\Leftrightarrow m=0,72\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}15V-28m=0\\m=0,72\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m=0,72\left(g\right)\\V=1,344\left(l\right)\end{matrix}\right.\)