
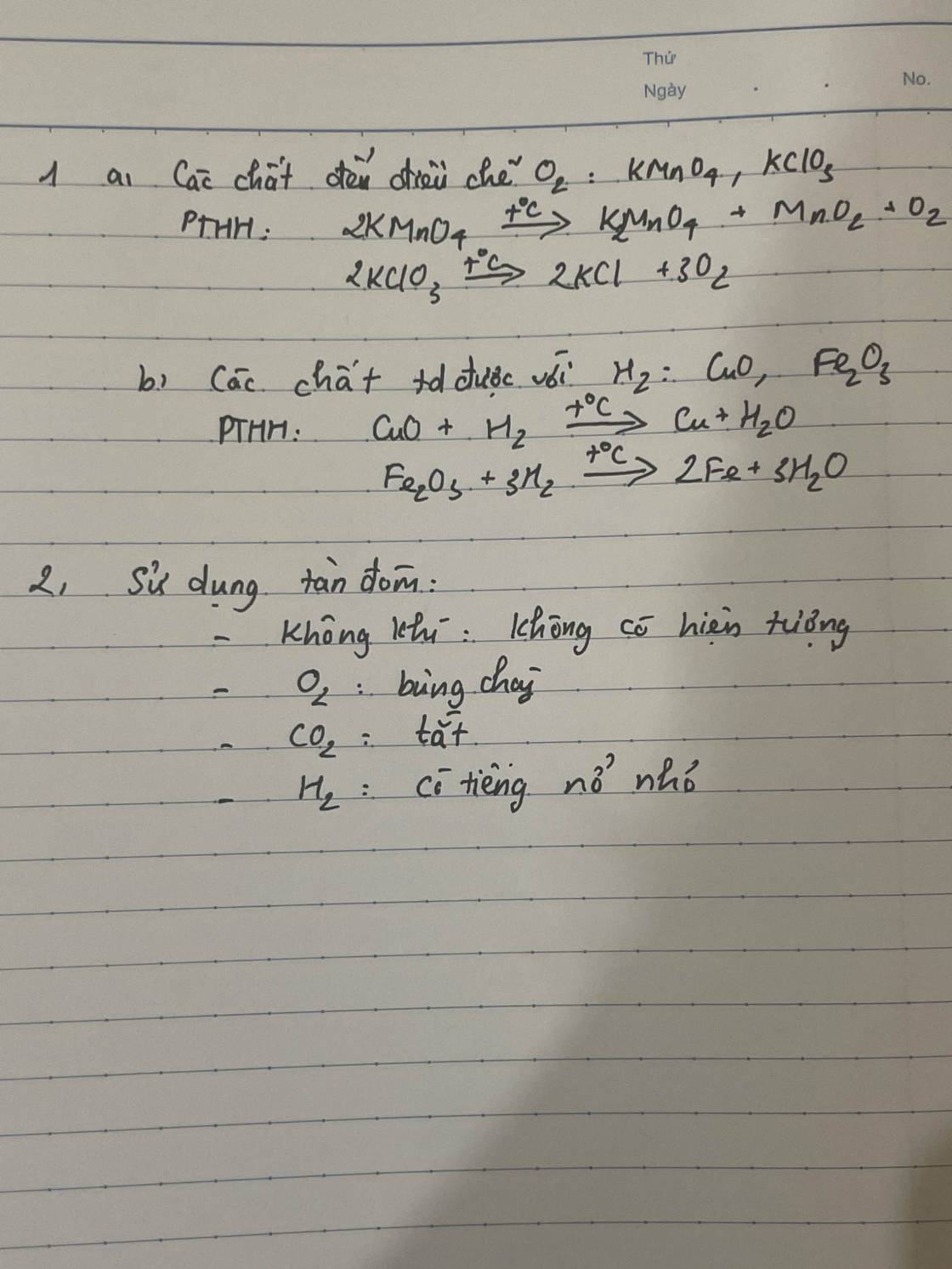
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

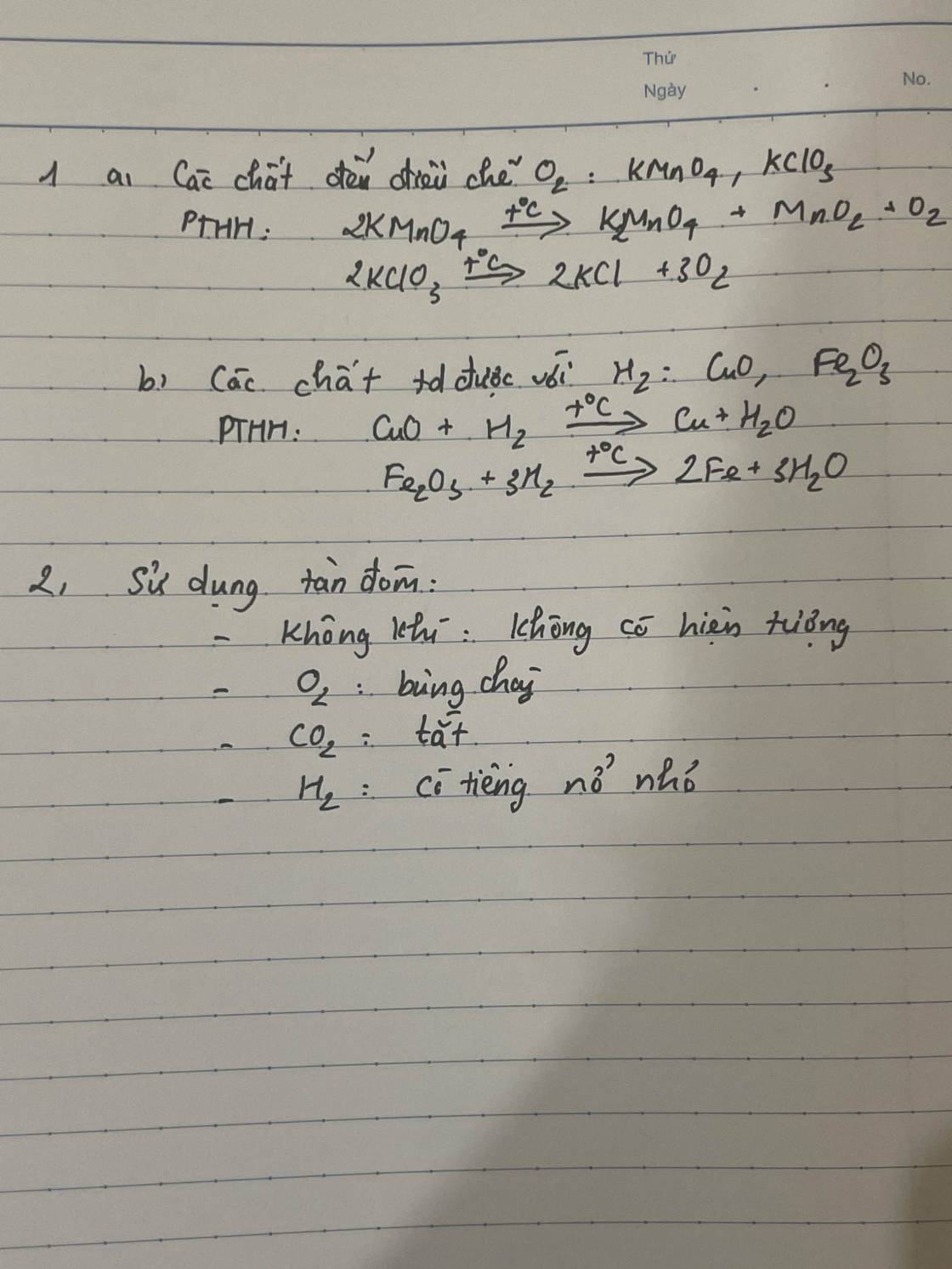

a)
\(2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\)
b) Tác dụng với
\(H_2O : CO_2,P_2O_5,CaO\\ CO_2 + H_2O \rightleftharpoons H_2CO_3\\ P_2O_5 + 3H_2O \to 2H_3PO_4\\ CaO + H_2O \to Ca(OH)_2\)
c) Đục nước vôi trong :\(CO_2\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
d) Tác dụng với H2
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\)
*) Các chất nhiệt phân ra O2:
2KClO3 --t°--> 2KCl + 3O2
2KMnO4 --t°--> K2MnO4 + MnO2 + O2*)
Chất tác dụng với H2O:
P2O5 + 3H2O -> 2H3PO4
CaO + H2O -> Ca(OH)2*)
Chất tác dụng với H2:
CuO + H2 --t°-> Cu + H2O
Fe2O3 + H2 --t°-> Fe + H2O*)
Chất àm đục nước vôi
CO2 + Ca(OH)2 --> CaCO3 + H2O
P2O5 + H2O --> H3PO4 , rồi sau đó làm đục nước vôi bằng ptpu:
2H3PO4 + 3Ca(OH)2 --> Ca3(PO4)2 + 6H2O

Đốt một que đóm còn tàn đỏ để vào ba bình:
-Nếu que đóm bốc cháy thì đó là bình chứa oxi.
-Nếu que đóm cháy một lúc rồi tắt thì đó là bình chứa không khí.
- Còn lại là bình chứa H2.

Bài 1.
Sục 3 khí vào dd Ca(OH)2
-CO2: xuất hiện kết tủa trắng
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
-O2,H2,kk: ko hiện tượng
Dùng que đóm đang cháy đưa vào 3 lọ:
-O2: cháy mãnh liệt
-H2: cháy với ngọn lửa xanh, nổ nhẹ
-kk: cháy bình thường
Bài 2.
a.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
\(2Cu+O_2\rightarrow\left(t^o\right)CuO\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
b.
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
Dùng que đóm cho nhanh
- Cháy mãnh liệt O2
- Cháy màu xanh nhạt H2
- Cháy yếu kk
- Vụt tắt CO2
Chứ bạn ấy đã học CaCO3 có kết tủa trắng đâu :) chứ ko phải là em sai

a, 2KClO3 -> (t°, MnO2) 2KCl + 3O2
b, BaO + H2O -> Ba(OH)2
c, ZnO + H2 -> (t°) Zn + H2O
Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O
a, 2KClO3 -> (t°, MnO2) 2KCl + 3O2
b, BaO + H2O -> Ba(OH)
c, ZnO + H2 -> (t°) Zn + H2O
Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O

\(2K+2H_2O->2KOH+H_2\\
2Na+2H_2O->2NaOH+H_2\\
Ca+2H_2O->Ca\left(OH\right)_2+H_2\\
Ba+2H_2O->Ba\left(OH\right)_2+H_2\\
2Li+2H_2O->2LiOH+H_2\\
CaO+H_2O->Ca\left(OH\right)_2\\
Na_2O+H_2O->2NaOH\\
BaO+H_2O->Ba\left(OH\right)_2\\
P_2O_5+3H_2O->2H_3PO_4\\
SO_3+H_2O->H_2SO_4\)
\(O_2+2H_2-t^o->2H_2O
\\
CuO+H_2-t^O->Cu+H_2O\\
Fe_2O_3+3H_2-t^O->2Fe+3H_2O\\
PbO+H_2-t^O->Pb+H_2O\\
Fe_3O_4+4H_2-t^O->3Fe+4H_2O\)
a/
\(2K+2H_2O\rightarrow2KOH+H_2\\ 2Na+2H_2O\rightarrow2NaOH+H_2\\ Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\\ Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\\ 2Li+H_2O\rightarrow2LiOH+H_2\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2+H_2\\ Na_2O\rightarrow2NaOH\\ BaO+H_2O\rightarrow Ba\left(OH\right)_2\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ SO_3+H_2O\rightarrow H_2SO_4\)
b/
\(2H_2+O_2\underrightarrow{t^o}2H_2O\\ CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ PbO+H_2\underrightarrow{t^o}Pb+H_2O\\ Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\\ Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)