Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
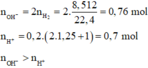
=> Kết tủa chứa BaSO4 và Al(OH)3.
• Có 24 , 86 + 30 , 08 = m KL + m OH - trong Al ( OH ) 3 + m SO 4 2 - + m Cl -
=> m + 17(0,76 - 0,7) + 96.0,25 + 35,5.0,2 = 54,94 g
=> m = 22,82 g
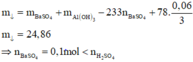
=> Chứng tỏ Ba2+ tạo kết tủa hoàn toàn: n Ba = 0 , 1 mol
![]()

Đáp án A
Theo quy tắc đường chéo tính đươc N2O :0,01 mol và NO : 0,03 mol
Đặt nMg =x và nFe3O4= y mol. Số mol NH4NO3 là a mol
Ta có mX = 24x + 232y =9,6
Bảo toàn e : 2x + y = 0,01.8 + 0,03.3 + 8a
nHNO3(dư) =0,04 mol. Bảo toàn N ta có 2x + 3.3y +2a + 0,01.2 + 0,03 + 0,04= 0,6
Giải được x =0,11 ; y =0,03 ; a=0,01
Ta có mmuối=0,11 .148 + 0,03.3.242 + 0,01.80 +0,04.85 =42,26g

nếu HCl dư=> chỉ có 3 chất tan
Nếu HCl đủ=> chỉ có 2 chất tan
=> HCl thiếu => 2 muối và 2 dd kiềm
thay vào để giải nghiệm thì chỉ có Li và K thỏa mãn=> 2 kim loại cần tìm là Liti vs Kali

Đáp án C
2107 gam dung dịch H2SO4 loãng, nồng độ 10% gồ 2,15 mol chất tan H2SO4 và 189,3 gam H2O.
→ kết quả cô cạn dung dịch Y thu được 1922,4 gam H2O là gồm lượng sẵn có trên là lượng sinh ra thêm do phản ứng giữa X + H 2 SO 4 ⇒ lượng sinh thêm là 26,1 gam ⇄ 1,45mol
*Sơ đồ phản ứng:
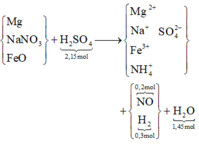
Có sơ đồ, việc giải bài tập trở nên đơn giản, chỉ là thuần “ban bật” bảo toàn nguyên tố qua dấu “ → ”:
Thật vậy, bảo toàn nguyên tố H có 0,2 mol NH 4 + → có 0,4 mol NaNO3 theo bảo toàn nguyên tố N.
Bỏ góc SO4 hai vế rồi bảo toàn nguyên tố O có 0,45 mol
![]()
Mà oxi chiếm 26,4% khối lượng X nên
![]()
Biết lượng FeO, NaNO3 rồi nên suy ra lượng còn lại 33,6 gam là của Mg.
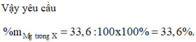

Đáp án B
Giả sử KOH không dư ⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí! ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g)
16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16
⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
-> nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol
⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%

Giả sử KOH không dư
⇒ nKNO2 = nKOH = 0,5 mol
⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí!. ⇒ KOH dư.
Đặt nKNO3 = x; nKOH dư = y.
Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư
⇒ 85x + 56y = 41,05
⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
● Đặt nFe = a; nCu = b
⇒ mA = 56a + 64b = 11,6(g)
16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16
⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol.
Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol.
Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
⇒ Bảo toàn khối lượng:
mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
► nNO3–/X < 3nFe + 2nCu
⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol
⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%
Đáp án B


