Hỗn hợp khí X gồm H2 và O2 có tỉ khối của X so với hydrogen là 8,5. Tính số mol mỗi khí có trong 7,437 lít (đkc) hỗn hợp X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tính chất giống nhau
- Đều có tính oxi hoá
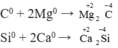
- Đều có tính khử
Tác dụng với phi kim
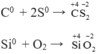
Tác dụng với hợp chất:
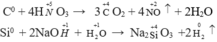

Axit nitric và axit sunfuric đặc đều có tính oxi hóa mạnh.
Ví dụ: 3FeO +10HNO3 —> 3Fe(NO3)3 + NO ↓+ 5H2O
2FeO + 4H2SO4 —> Fe2SO4)3 + SO2 + 4H2O
Tuy nhiên nếu như HNO3 loãng vẫn có tính oxi hóa thì H2SO4 loãng lại không có tính oxi hóa. Ví dụ
3Fe3O4 + 28HNO3 l -> 9Fe(NO3)3 + NO↓+ 14H2O Fe3O4 + 4H2SO4 l —> FeSO4 + Fe2(S04)3 + 4H2O

b1:
PTHH: \(S+O_2\Rightarrow SO_2\)
b2:
nSO2=\(\dfrac{m}{M}=\dfrac{4}{64}=0,0625mol\)
b4:
VSO2=22,4.n=22,4.0,0625=1,4 (lít)

Tính chất hóa học của nước :
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường :
Pt : Ca + 2H2O \(\rightarrow\) Ca(OH)2 + H2
Na + 2H2O \(\rightarrow\) 2NaOH + H2
Tác dụng với oxit bazo :
Pt : CaO + H2O \(\rightarrow\) Ca(OH)2
K2O + H2O \(\rightarrow\) 2KOH
Tác dụng với oxit axit
Pt : SO3 + H2O \(\rightarrow\) H2SO4
P2O5 + 3H2O \(\rightarrow\) 2H3PO4
Chúc bạn học tốt
Tính chất hh của nước:
✱Tác dụng với kim loại:
VD: Na + H2O → NaOH + \(\dfrac{1}{2}\)H2↑
Ca + 2 H2O → CaOH + H2↑
✱Tác dụng với oxit bazơ:
VD: K2O + H2O → KOH
BaO + H2O → Ba(OH)2
✱Tác dụng với oxit axit:
VD: CO2 + H2O → H2CO3
SO2 + H2O → H2SO3

Tác dụng với kim loại
\(Mg+FeSO_4\rightarrow MgSO_4+Fe\)
Tác dụng với axit:
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
Tác dụng với dd bazo:
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Tác dụng vơi dd muối:
\(NaCl+AgNO_3\rightarrow AgCl+NaNO_3\)
Phản ứng phân hủy muối:
\(CaCO_3\xrightarrow[]{t^0}CaO+CO_2\)
`#3107.101107`
`@` Tính Chất Hóa Học của Muối:
`1)` Phản ứng với Kim Loại
Kim Loại + Muối `\rightarrow` Muối Mới + Kim Loại Mới
\(\text{Fe + CuSO}_4\rightarrow\text{ FeSO}_4+\text{Cu}\)
`2)` Phản ứng với Acid
Acid + Muối `\rightarrow` Muối Mới + Acid Mới
Điều kiện: sản phẩm có chất kết tủa hoặc có khí
\(\text{BaCl}_2+\text{H}_2\text{SO}_4\rightarrow\text{ BaSO}_4+\text{2HCl}\)
`3)` Phản ứng với muối
Muối + Muối `\rightarrow` 2 Muối Mới
Điều kiện: sản phẩm kết tủa
\(\text{BaCl}_2+\text{Na}_2\text{SO}_4\rightarrow\text{ BaSO}_4+\text{ 2NaCl}\)
`4)` Phản ứng với base
Muối + Base `\rightarrow` Muối Mới + Base Mới
\(\text{CuSO}_4+\text{2NaOH}\rightarrow\text{ Cu(OH)}_2+\text{Na}_2\text{SO}_4.\)
Ta có: \(n_{H_2}+n_{O_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\) (1)
- Tỉ khối của X so với H2 là 8,5.
\(\Rightarrow\dfrac{2n_{H_2}+32n_{O_2}}{n_{H_2}+n_{O_2}}=8,5.2\) \(\Rightarrow2n_{H_2}+32n_{O_2}=8,5.2.0,3\left(2\right)\)
Từ (1) và (2) ⇒ nH2 = nO2 = 0,15 (mol)