Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau: Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 thu được 3,36 lít H₂(ở đktc). Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (ở đktc). Giá trị của V
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

4 tháng 1 2017
Đáp án A
Vì hai kim loại X, Y đều có hóa trị không đổi và khối lượng hai phần bằng nhau nên ở hai phần, số mol electron mà kim loại nhường bằng nhau.
Khi đó
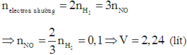

10 tháng 4 2016
mKL 1phần = 5gTN1: td với \(O_2\)Bảo toàn klg\(\Rightarrow m_{O_2}\)=5,32-5=0,32g\(\Rightarrow mol\) \(O_2\)=0,01 mol\(\Rightarrow\)V=0,224l\(O_2+4e\rightarrow2O_2-\)0,01 mol\(\Rightarrow\)0,04 molMol e nhận=0,04 molP2: lượng KL vẫn thế\(\Rightarrow\)mol e nhận và nhường ko đổi=0,04 mol\(2H++2e\rightarrow H_2\)0,04 mol\(\Leftarrow\)0,04 mol\(\Rightarrow\)0,02 molV'=0,02.22,4=0,448lMol \(HCl\)=2mol\(H_2\)=0,04 mol\(\Rightarrow\)\(m_{HCl}\)=1,46gBảo toàn klg=>m=5+1,46-0,02.2=6,42g

13 tháng 1 2022
\(1)n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ Mg+2HCl\to MgCl_2+H_2\\ Fe+2HCl\to FeCl_2+H_2\)
Từ giả thiết và theo PT:
\(\begin{cases} 24n_{Mg}+56n_{Fe}=5,2\\ n_{Mg}+n_{Fe}=0,15 \end{cases}\\ \Rightarrow n_{Mg}=0,1(mol);n_{Fe}=0,05(mol)\)
\(\Rightarrow \begin{cases} \%m_{Mg}=\dfrac{0,1.24}{5,2}.100\%=46,15\%\\ \%m_{Fe}=100-46,15=53,85\% \end{cases}\\ 2)\Sigma n_{HCl}=2n_{H_2}=0,3(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,3}{1}=0,3(l)=300(ml)\)
13 tháng 1 2022
lười làm thì đừng làm
box hóa có luật không tham khảo rồi




