a) Hiệu suất phản ứng được tính bằng cách nào?
b) Khi nào hiệu suất của phản ứng bằng 100%?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTHH: \(KMnO_4\rightarrow^{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
b. \(H=100\%\)
\(n_{KMnO_4}=\frac{3,6}{158}=0,023mol\)
Theo phương trình \(n_{O_2}=0,5n_{KMnO_4}=0,046mol\)
\(\rightarrow V_{O_2}=0,0115.22,4.100\%=0,2576l\)
c. H = 80%
\(\rightarrow V_{O_2}=0,0115.22,4.80\%=0,20608l\)

$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
$a\bigg)$
$n_{KMnO_4}=\frac{15,8}{158}=0,1(mol)$
Chất rắn sau p/ứ là $K_2MnO_4,MnO_2$
Theo PT: $n_{K_2MnO_4}=n_{MnO_2}=0,05(mol)$
$\to m_{\rm chất\, rắn}=0,05.197+0,05.87=14,2(g)$
$b\bigg)$
Vì $H=80\%\to n_{KMnO_4(p/ứ)}=0,1.80\%=0,08(mol)$
$\to n_{KMnO_4(dư)}=0,02(mol)$
Chất rắn sau p/ứ là $KMnO_4(dư):0,02;K_2MnO_4:0,04;MnO_2:0,04$
$\to m_{\rm chất\, rắn}=0,02.158+0,04.197+0,04.87=14,52(g)$
$c\bigg)$
Bảo toàn KL có:
$m_{O_2}=m_{KMnO_4}-m_{CR}$
$\to m_{O_2}=15,8-14,68=1,12(g)\to n_{O_2}=0,035(mol)$
Theo PT: $n_{KMnO_4(p/ứ)}=2n_{O_2}=0,07(mol)$
$\to H=\dfrac{0,07}{0,1}.100\%=70\%$

Chọn B
Thay O2 không khí bằng O2 tinh khiết là làm tăng nồng độ của O2. Trường hợp này cân bằng chuyển dịch theo chiều thuận, do đó làm tăng hiệu suất của phản ứng.
Tăng áp suất thì cân bằng hóa học sẽ chuyển dịch theo chiều làm giảm số phân tử khí, tức là chiều thuận, do đó cũng làm tăng hiệu suất tổng hợp SO3.
Chất xúc tác không làm ảnh hưởng đến sự chuyển dịch cân bằng, nó chỉ giúp cho cân bằng nhanh chóng được thiết lập.
Tăng nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều thu nhiệt, tức là chiều nghịch, do đó làm giảm hiệu suất phản ứng.
Vậy các biện pháp (a) và (b) là tăng hiệu suất phản ứng

\(a,n_{CH_3COOC_2H_5}=\dfrac{11}{88}=0,125\left(mol\right)\)
PTHH: \(CH_3COOH+C_2H_5OH\xrightarrow[t^o]{H_2SO_{4\left(đ\right)}}CH_3COOC_2H+H_2O\)
0,125<------------------------------0,125
b, => mCH3COOH = 0,125.60 = 7,5 (g)
\(c,H=\dfrac{7,5}{12}.100\%=62,5\%\)
a.b.\(n_{CH_3COOC_2H_5}=\dfrac{11}{88}=0,125mol\)
\(CH_3COOH+C_2H_5OH\rightarrow\left(t^o,H_2SO_4\left(đ\right)\right)CH_3COOC_2H_5+H_2O\)
0,125 0,125 ( mol )
\(m_{CH_3COOH}=0,125.60=7,5g\)
c.\(n_{CH_3COOH}=\dfrac{12}{60}=0,2mol\)
\(H=\dfrac{0,125}{0,2}.100\%=62,5\%\)

đề bảo "pư đạt trạng thái cân bằng" chứ không phải "phản ứng hoàn toàn" nên cần thêm dữ kiện để tính câu b) á :v

Ta có: dhỗn hợp/H2 = 4,44 ⇒ Mhỗn hợp = 4,44.2 = 8,88
Gọi nCH4 ban đầu là là 1
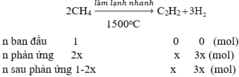
Tổng số mol khí sau phản ứng: 1 - 2x + x + 3x = 1 + 2x (mol)
MX = 2. 4,44 = 8,88
Áp dụng định luật bảo toàn khối lượng ta có:
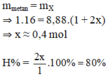

Chọn B.
Với 1 mol A và 1 mol B, lúc cân bằng hiệu suất phản ứng đạt 66,67% nên: nA = nB = 0,3333 mol; nC = nD = 0,6667 mol.
Do đó: Kc = Kp = Kx = 4.

C1
\(m_{KClO_3\left(pư\right)}=\dfrac{24,5.60}{100}=14,7\left(g\right)\)
\(n_{KClO_3\left(pư\right)}=\dfrac{14,7}{122,5}=0,12\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,12--------->0,12--->0,18
=> \(m_{O_2}=0,18.32=5,76\left(g\right)\)
C2: \(m_{KCl}=0,12.74,5=8,94\left(g\right)\)
Theo ĐLBTKL: \(m_{KClO_3\left(pư\right)}=m_{KCl}+m_{O_2}\)
=> \(m_{O_2}=14,7-8,94=5,76\left(g\right)\)
a, Hiệu suất phản ứng được tính theo 1 trong 3 CT sau:
\(H=\dfrac{m_{thực.tế}}{m_{lý.thuyết}}.100\%;H=\dfrac{n_{thực.tế}}{n_{lý.thuyết}}.100\%;H=\dfrac{V_{thực.tê}}{V_{lý.thuyết}}.100\%\)
b, Hiệu suất của phản ứng bằng 100% khi không có hao hụt trong và sau phản ứng, lượng chất sản phẩm thực tế bằng lượng chất sản phẩm lý thuyết.