đốt cháy hoàn toàn 9g chất hữu cơ A thu được 13.2g khí CO2 và 5.4g nước. Xác định công thức phân tử của A, biết tỷ khối của A so với hidro bằng 30
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có MA=46x2=92g/mol
nCO2=0.44:4=4=0.01 (mol)
nH2O=0.27:18=0.015(mol)
trong phân tử chắn chắn có C, H và có thể có O
=>mO=0.23-0.015x2-0.01x12=0.08g
-->nO=0.08:16=0.005(mol)
Nên trong hợp chất có cả C,H và O
Gọi CTDGN (CxHyOz)n
ta có x:y:z=0.01:0.03:0.005=2:6:1
nên CTDGN (C2H6O)n=46n=92----->n=2
CTPT A là C4H12O2
\(n_{CO_2}=n_C=0,01\)
\(n_{H_2O}=0,015\Rightarrow n_H=0,03\)
\(n_O=\dfrac{m_A-12n_C-n_H}{16}=0,005\)
\(n_C:n_H:n_O=0,01:0,03:0,005=2:6:1\)
\(\Rightarrow\left(C_2H_6O\right)_n\)
Mà \(M_A=46\cdot2=92\)
\(\Rightarrow M_{C_2H_6O}\cdot n=92\Rightarrow46n=92\Rightarrow n=2\)
Vật CTPT của A là \(C_4H_{12}O_2\)

a)
\(n_{CO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn C: nC = 0,375 (mol)
Bảo toàn H: nH = 0,9 (mol)
mC = 0,375.12 = 4,5 (g)
mH = 0,9.1 = 0,9 (g)
=> mO = 5,4 - 4,5 - 0,9 = 0 (g)
=> \(\left\{{}\begin{matrix}\%C=\dfrac{4,5}{5,4}.100\%=83,33\%\\\%H=\dfrac{0,9}{5,4}.100\%=16,67\%\end{matrix}\right.\)
b)
nC : nH = 0,375 : 0,9 = 5 : 12
=> CTDGN: C5H12
c)
CTPT: (C5H12)n
Mà M = 2,25.32 = 72 (g/mol)
=> n = 1
=> CTPT: C5H12

a)
\(n_{CO_2} = \dfrac{26,4}{44} = 0,6(mol)\\ n_{H_2O} = \dfrac{16,2}{18} = 0,9(mol)\\ n_{O_2} = \dfrac{26,4+16,2-9}{32} = 1,05(mol)\\ \Rightarrow n_{O(trong\ A)} = 2n_{CO_2} + n_{H_2O} - 2n_{O_2} = 0\)
Vậy A gồm 2 nguyên tố : Cacbon và Hidro
b)
\(n_C = n_{CO_2} = 0,6(mol)\\ n_H = 2n_{H_2O} = 1,8(mol)\\ n_A = \dfrac{9}{30} = 0,3(mol)\)
Số nguyên tử Cacbon = \(\dfrac{n_C}{n_A} = \dfrac{0,6}{0,3} = 2\\ \)
Số nguyên tử Hidro = \(\dfrac{n_H}{n_A} = \dfrac{1,8}{0,3} = 6\)
Vậy CTPT của A : C2H6.

\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Bảo toán C: nC(A) = 0,15 (mol)
Bảo toàn H: nH(A) = 0,2.2 = 0,4 (mol)
=> \(n_O=\dfrac{2,2-0,15.12-0,4.1}{16}=0\left(mol\right)\)
Xét nC : nH = 0,15 : 0,4 = 3:8
=> CTPT: (C3H8)n
Mà MA = 22.2 = 44(g/mol)
=> n = 1
=> CTPT: C3H8

\(n_{CO_2} = \dfrac{224}{1000.22,4} = 0,01(mol)\\ n_{H_2O} = \dfrac{0,18}{18} = 0,01(mol)\\ \Rightarrow n_{O_2} = \dfrac{0,01.44+0,18-0,3}{32} = 0,01\\ \Rightarrow n_{O(trong\ A)} = 2n_{CO_2} + n_{H_2O} - 2n_{O_2} = 0,01\\ n_C = n_{CO_2} = 0,01\\ n_H = 2n_{H_2O} = 0,02\\ n_A = \dfrac{0,3}{30,2} = 0,005(mol)\)
Số nguyên tử Cacbon = \(\dfrac{n_C}{n_A} = \dfrac{0,01}{0,005} = 2\)
Số nguyên tử Hidro = \(\dfrac{n_H}{n_A} = \dfrac{0,02}{0,005} = 4\)
Số nguyên tử Oxi = \(\dfrac{n_O}{n_A} = \dfrac{0,01}{0,005} = 2\)
Vậy CTPT của A: \(C_2H_4O_2\)

Ta có: \(d_{A/H_2}=100\)
\(\Rightarrow M_A=100.2=200\left(g/mol\right)\)
\(\Rightarrow n_A=\dfrac{2}{200}=0,01\left(mol\right)\)
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
⇒ Số nguyên tử C trong A là: \(\dfrac{0,1}{0,01}=10\)
\(n_{H_2O}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\Rightarrow n_H=0,08.2=0,16\left(mol\right)\)
⇒ Số nguyên tử H trong A là: \(\dfrac{0,16}{0,01}=16\)
Giả sử n là số nguyên tử O có trong A.
Ta có: 10.12 + 16 + n.16 = 200
⇒ n = 4
Vậy: CTPT của A là C10H16O4.
Bạn tham khảo nhé!
Bảo toàn nguyên tố với C,H :
\(n_C = n_{CO_2} = \dfrac{4,4}{44}= 0,1(mol)\\ n_H = 2n_{H_2O} = 2.\dfrac{1,792}{22,4} = 0,16(mol)\)
Mà :
\(m_O = m_A - m_C - m_H = 2 - 0,1.12 - 0,16 = 0,64(gam)\\ \Rightarrow n_O = \dfrac{0,64}{16} = 0,04(mol)\)
Ta có :
\(n_C: n_H : n_O = 0,1 :0,16 : 0,04 = 5 : 8 : 2\)
Vậy CTPT của A là : \((C_5H_8O_2)_n\)
Mà :
\(M_A = (12.5+8+16.2)n = M_{H_2}.100 = 200(đvC)\\ \Rightarrow n = 2\)
Vậy CTPT của A : \(C_{10}H_{16}O_4\)

\(n_C=\dfrac{2,2}{44}=0,05\left(mol\right)\\ n_H=2.\dfrac{1,35}{18}=0,15\left(mol\right)\\ n_O=\dfrac{1,15-0,05.12-0,15}{16}=0,025\left(mol\right)\)
\(CTPT:C_xH_yO_z\\ \Rightarrow x:y:z=0,05:0,15:0,025=2:6:1\\ \Rightarrow\left(C_2H_6O\right)_n=1,4375.32=46\left(\dfrac{g}{mol}\right)\\ \Rightarrow n=1\\ CTPT:C_2H_6O\)

Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam) Trong A có 3 nguyên tố C,H,O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
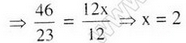
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O

Theo gt ta có: $n_{CO_2}=0,2(mol);n_{H_2O}=0,3(mol)$
Chất A có CTTQ là $C_xH_y$ (vì có 2 nguyên tố)
Ta có: $x:y=0,2:0,6=1:3$
Vậy CTĐGN của A là $(CH_3)_n$
Mà $M_A=30\Rightarrow A=C_2H_6$
\(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,6.1 = 4,2 (g) < mA
→ A gồm C, H và O.
⇒ mO = 9 - 4,2 = 4,8 (g) \(\Rightarrow n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,3:0,6:0,3 = 1:2:1
→ CTPT của A có dạng (CH2O)n
Mà: MA = 30.2 = 60 (g/mol)
\(\Rightarrow n=\dfrac{60}{12+1.2+16}=2\)
Vậy: CTPT của A là C2H4O2