1 hợp chất A tạo bởi 1 nguyên tử B vá 2 nguyên tử H có khối lượng bằng khối lượng phân tử O(2O) xác định nguyên tử khối của B và phân tử khối của A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Mình trình bày ko đc tốt cho lắm nhé (nt:nguyên tử)
a. Trong hợp chất A :
số ntử của C = 42,6 * PTK(A) / 16 *100
số nguyên tử O = 57,4* PTK(A) / 16*100
từ đó suy ra số nt C/số nt O = 1
cậu làm tương tư trong hợp chất B nhé kết quả là số ntC/số nt O =2
b. PTK(A) là12+16=28đv C
PTK (B) là 12+16*2=44đvC

Gọi ct chung: \(H_xO_y\)
\(K.L.P.T=1.x+16.y=18< amu>.\)
\(\%H=\dfrac{1.x.100}{18}=11,11\%\)
\(H=1.x.100=11,11.18\)
\(H=1.x.100=199,98\)
\(1.x=199,98\div100\)
\(1.x=1,9998\)
\(\Rightarrow\)\(x=1,9998\) làm tròn lên là 2
vậy, có 2 nguyên tử H trong phân tử \(H_xO_y\)
\(\%O=\dfrac{16.y.100}{18}=88,89\%\)
\(\Rightarrow y=1,00...\) làm tròn lên là 1 (cách làm tương tự).
Vậy, có 1 nguyên tử O trong phân tử trên
\(\Rightarrow CTHH:H_2O.\)

Gọi công thức của A là H 3 X O y (vì nhóm X O y hóa trị III nên theo quy tắc hóa trị ta xác định được phân tử có 3 nguyên tử H)
Phân tử khối của H 2 S O 4 : 2 + 32 + 16.4 = 98 (đvC)
Vì A nặng bằng phân tử H 2 S O 4 nên PTK của A là 98 đvC
Theo đề bài, ta có khối lượng của nguyên tố oxi trong hợp chất là:
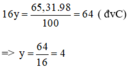
→ có 4 nguyên tử oxi trong hợp chất A.
Vậy nguyên tử khối của X là: 98 – (3 + 64) = 31 (đvC)

Gọi CTHH A, B lần lượt là: CxOy và CmOn
Ở h/c A: 12x/ 16y = 42,6/57,4
=> x: y= 1: 1
Vậy CTHH của A là: CO
=> PTK A = 28
Ở h/c B : 12m/ 16n = 27,3/72,7
=> m: n= 1: 2
Vậy CTHH B là: CO2
=> PTK B = 44

a) M = 2.40 = 80 (g/mol)
b) CTHH: XO3
=> MX + 3.16 = 80
=> MX = 32(S)
=> CTHH: SO3
nguyên tử khối của B là 30 amu
phân tử khối của A là 32 amu