Trong hai chất nh3 và H2S hãy cho biết chất nào có nhiệt độ sôi cao hơn. Hãy giải thích tại sao
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


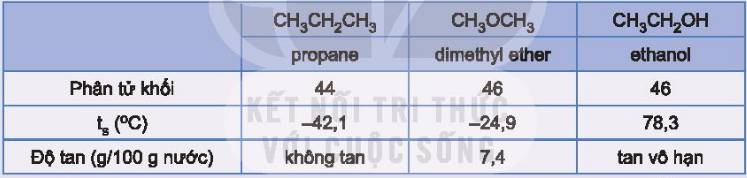
Do các phân tử ethanol có thể tạo liên kết hydrogen với nhau và với nước.

Nhiệt độ sôi của hydrogen bromide cao hơn nhiệt độ sôi của hydrogen chloride được giải thích như sau:
+ Khối lượng phân tử HBr (81) cao hơn khối lượng phân tử HCl (36,5)
+ Br có bán kính nguyên tử lớn, có nhiều electron hơn Cl => Tăng khả năng lưỡng cực HX => Làm tăng tương tác van der Waals giữa các phân tử

Theo nguyên tử khối của Halogen, ta sẽ có: \(M_F< M_{Cl}< M_{Br}< M_I\)
Do đó: Nhiệt độ sôi tương ứng của chúng sẽ tăng dần
=> Nhiệt độ sôi của CH3F, CH3Cl, CH3Br, CH3I lần lượt là -78 độ C, -24 độ C, 4 độ C và 24 độ C

Dự đoán nhiệt độ sôi các chất như sau:
Chất | C2H6 | C2H5Cl | C2H5OH | C6H5CH2OH |
to sôi | -89 oC | 12,3 oC | 78,3 oC | 205 oC |
Giải thích dự đoán:
- Do tạo được liên kết hydrogen liên phân tử nên các alcohol có nhiệt độ sôi cao hơn các hydrocarbon hoặc dẫn xuất halogen có phân tử khối tương đương.
- Nhiệt độ sôi của các alcohol tăng dần khi phân tử khối tăng.

Dự đoán nhiệt độ sôi các chất như sau:
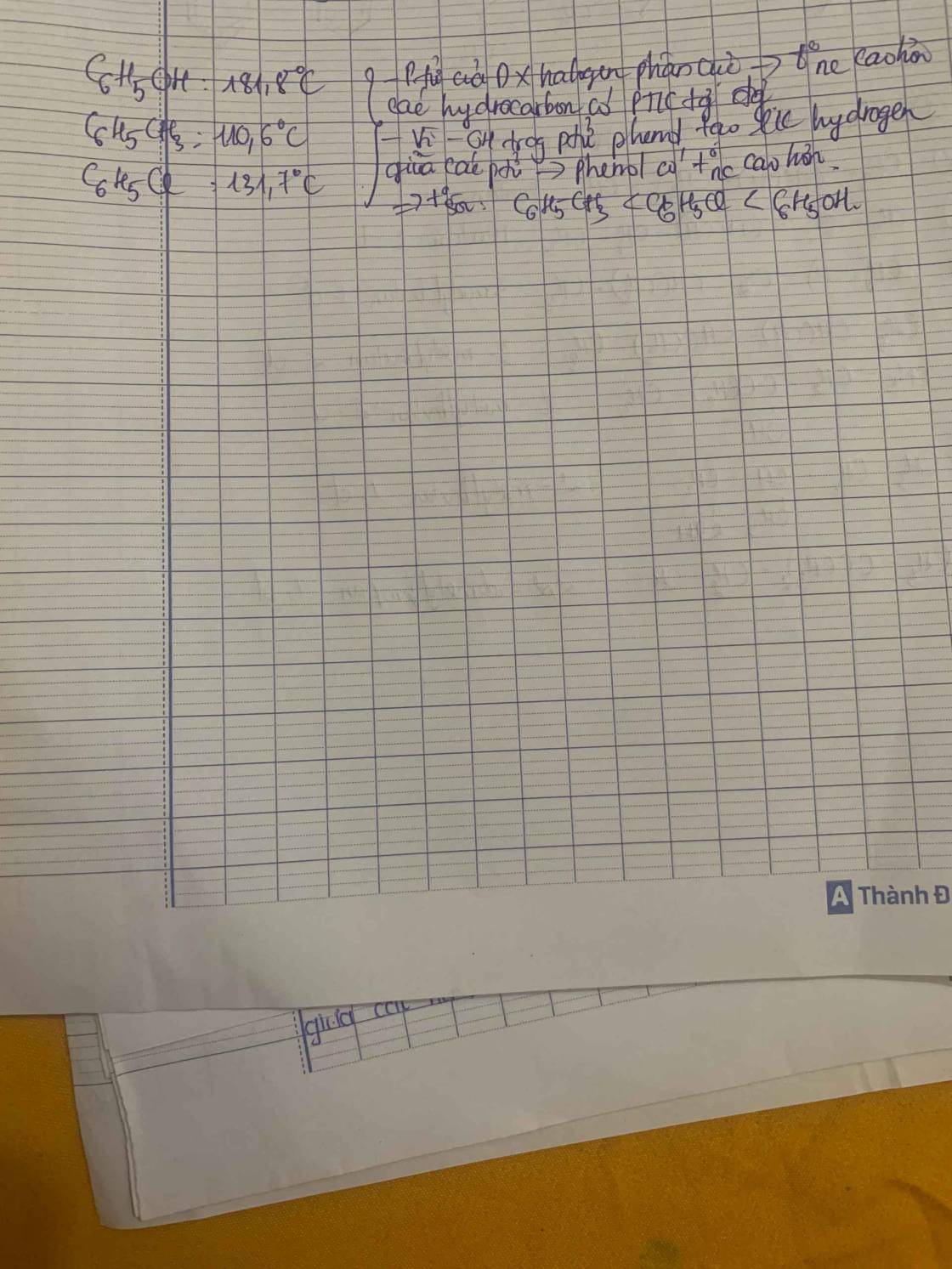
Chất | C6H5CH3 | C6H5Cl | C6H5OH |
Nhiệt độ sôi | 110 oC | 132 oC | 182 oC |
Giải thích:
- Do có nhóm – OH trong phân tử nên phenol tạo ra liên kết hydrogen giữa các phân tử. Do vậy, phenol có nhiệt độ sôi cao hơn C6H5Cl (có phân tử khối tương đương).
- Do liên kết C – Cl phân cực nên C6H5Cl có nhiệt độ sôi cao hơn C6H5CH3 (có phân tử khối tương đương).

Đặc điểm hợp chất ion:
+ Các hợp chất ion thường là tinh thể rắn ở điều kiện thường
+ Hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi rất cao
=> Phát biểu (b) và (c) đúng