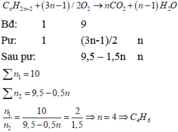Để xác định thành phần của một hỗn hợp gồm khí butan (c4h10) và hơi pentan (CH2) người ta cho 10 cm3 hỗn hợp đó và 90 cm khí O2 vào bình kín. Sau khi bật tia lửa điện để đốt cháy hỗn hợp rồi đưa về điều kiện ban đầu người ta thấy các khí đó chiếm thể tích là 64,75 cm3 trong đó có 40,5 cm3 khí bị KOH hấp thụ, phần còn lại là khí O2 Xác định phần trăm thể tích của hỗn hợp khí ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D.
Đốt 35 ml (amin; H2) + 40 ml O2 → t o 10 ml CO2 + 5 ml N2 + 5 ml O2 dư.
Amin đơn chức.
⇒ Có 5 ml N2
→ Có 10 ml amin.
⇒ Trong 35 ml hỗn hợp còn 25 ml khí H2 nữa.
Chú ý: Đốt 10 ml amin cho 10 ml CO2
⇒ amin là C1 ứng với amin duy nhất là CH3NH2: metylamin.

Đáp án D
Ban đầu đặt thể tích H2 là x thì thể tích amin là 35-x ml
Sau phản ứng có 10 mol CO2 và 5 ml N2, 5 ml O2
40 ml O2 + (X, H2) → H2O, CO2 : 10 ml, N2: 5 ml và còn dư 5 ml O2
Từ sơ đồ thấy có 35ml O2 tham gia vào phản ứng
Vì amin này đơn chức nên Vamin = 2VN2 = 10ml nên số C trong X là 10 :10 =1

Đáp án D
Ban đầu đặt thể tích H2 là x thì thể tích amin là 35-x ml
Sau phản ứng có 10 mol CO2 và 5 ml N2, 5 ml O2
40 ml O2 + (X, H2) → H2O, CO2 : 10 ml, N2: 5 ml và còn dư 5 ml O2
Từ sơ đồ thấy có 35ml O2 tham gia vào phản ứng
Vì amin này đơn chức nên Vamin = 2VN2 = 10ml nên số C trong X là 10 :10 =1

Chọn đáp án D
Đốt 35 mL (amin; H2) + 40 mL O2 ―t0→ 10 mL CO2 + 5 mL N2 + 5 mL O2 dư
Amin đơn chức ⇒ có 5 mL N2 → có 10 mL amin ⇒ trong 35 mL hỗn hợp còn 25 mL khí H2 nữa.
Chú ý: đốt 10 mL amin cho 10 mL CO2 ⇒ amin là C1 ứng với amin duy nhất là CH3NH2: metylamin
⇒ chọn đáp án D

Đáp án A
Do điều kiện như nhau nên ta sử dụng thể tích như số mol (để tiện tính toán)
Ta có: 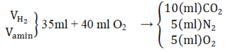
Amin đơn chức ⇒ Vamin = 2 V N 2 = 10 ml
⇒ V H 2 = 35 – 10 = 25 ml
⇒ Số C của amin là: V C O 2 V a m i n = 10 10 = 1
Trong các phương án đã cho chỉ có CH5N thỏa mãn