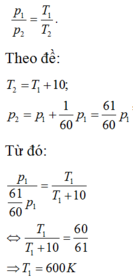Nếu lúc đầu người ta cho một nửa lượng khí lí tưởng đựng trong bình thoát ra ngoài và sau đó đốt nóng lượng khí còn lại đến nhiệt độ cao gấp hai lần nhiệt độ tuyệt đối ban đầu, thì khi đó áp suất trong bình sẽ thay đổi như thế nào sao với áp suất ban đầu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khi khí chưa thoát ra ngoài ta có: p 1 V 1 = m 1 μ R T 1 (1)
Khi một nửa lượng khí đã thoát ra ngoài ta có:
p 2 V 2 = m 2 μ R T 2 với V1 và m 2 = m 1 2 ⇒ p 2 V 1 = m 1 2 μ R T 2
Từ (1) và (2) ⇒ p 2 = p 1 T 2 2 T 1 = 40.285 2.300 = 19 a t m

Trạng thái 1: \(\left\{{}\begin{matrix}p_1=2\cdot10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\T_2=627^oC=900K\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{2\cdot10^5}{300}=\dfrac{p_2}{900}\)
\(\Rightarrow p_2=6\cdot10^5Pa\)

+ Khi khí chưa thoát ra ngoài ta có:
![]()
+ Khi một nửa lượng khí đã thoát ra ngoài ta có:
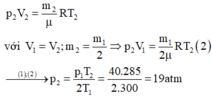

Ta có
Trạng thái 1: { V 1 p 1 = 1 , 5 a t m T 1 = 27 + 273 = 300 K Trạng thái 2: { V 2 = V 1 2 p 2 = ? T 2 = 273 + 127 = 400 K
Áp dụng
p 1 V 1 T 1 p 2 V 2 T 2 ⇒ p 2 = p 1 V 1 T 2 T 1 V 2 = 1 , 5. V 1 .400 300.0 , 5. V 1 p 2 = 4 ( a t m )

Xét lượng khí còn lại trong bình
Trạng thái 1: V 1 = V/2; T 1 = 27 + 273 = 300 K; p 1 = 40 atm.
Trạng thái 2: V 2 = V; T 2 = 12 + 273 = 285 K; p 2 = ? atm,
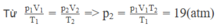

+ Gọi v 0 là thể tích của bình
Ta xét trạng thái của lượng khí còn lại trong bình sau khi nhiệt độ tăng lên 127 độ C. Khi đó nó chiếm thể tích cả binh nhưng khi chưa mả van và nhiệt độ trong binh còn 27 độ C thì nó chiếm một phần hai thể tích cả bình.
Khi lượng khí đó ở nhiệt độ 27 ° C trạng thái 1