1> một kim loại X chứa 64% Fe2O3, quặng Y chứa 69,6% Fe3O4. Trộn a tấn quặng X với b tấn quặng Y thu được một loại quặng Z có thể điều chế được 481,25 kg gang chứa 4% cacbon.( Gang là hợp chất của sắt và cacbon).
2> Phân hủy hoàn toàn một hợp chất A ở nhiệt độ cao theo phương trình sau:
4A nhiệt phân------> 4B+ C + 2D
Các sản phẩm tạo thành đều ở thể khí. Tính tỉ khối của hỗn hợp khí sau phản ứng so với khí hidro là 18. Xác định khối lượng mol của chất A
Các bạn giúp tui nha cám ơn mn nhiều:))
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

%Fe = 100% -4% = 96%
$m_{Fe} = 481,25.96% = 462(gam)$
$n_{Fe} = 462 : 56 = 8,25(kmol)$
Ta có : $a + b = 1(1)$
$m_{Fe_2O_3} = 1000a.64\% = 640a(kg)$
$\to n_{Fe_2O_3} = 640a : 160 = 4a(kmol)$
$m_{Fe_3O_4} = 1000b.69,6\% = 696b(kg)$
$\to n_{Fe_3O_4} = 696b : 232 = 3b(kmol)$
Bảo toàn nguyên tố với Fe :
$4a.2 + 3b.3 = 8,25(2)$
Từ (1)(2) suy ra a = 0,75(tấn) ; b = 0,25(tấn)

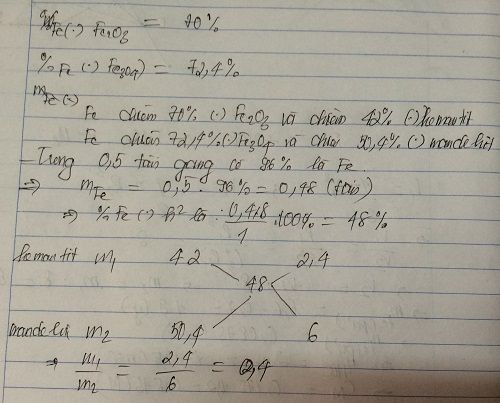
đề sai sai nha !
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4. Cần trộn X, Y theo tỉ lệ khối lượng như thế nào để được quặng Z mà từ 1 tấn quặng Z có thể điều chế được 0,5 tấn gang chứa 96% sắt?OK!

trong gang:nFe =3/350
BT ng tu ngto:2nFe2O3+3nFe3O4=3/350
=>2*0.6*m1/160+3*0.696*m2/232=3/350
m1+m2=1
=>m1=2/7;m2=5/7
=>m1:m2=2/5

%mFe ( trong A ) =
=> mFe ( trong A ) =
Vậy trong 1 tấn quặng A có chứa 420 kg Fe
%mFe ( trong B ) =
=> mFe ( trong B ) =
Vậy trong 1 tấn quặng B có chứa 504 kg Fe
%mFe2O3 =
%mFe3O4 =
=> mFe( quặng A trong C ) =
mFe ( quặng B trong C ) =
=> mFe ( trong C ) = 126 + 352,8 = 478,8 (kg)




2)
Giả sử có 1 mol A
PTHH: 4A --to--> 4B + C + 2D
1------->1-->0,25->0,5
=> nkhí sau pư = 1 + 0,25 + 0,5 = 1,75 (mol)
BTKL: mA = mB + mC + mD
Có \(\overline{M}=\dfrac{m_B+m_C+m_D}{1,75}=18.2=36\)
=> mA = 63 (g)
=> \(M_A=\dfrac{63}{1}=63\left(g/mol\right)\)
câu 1) đề có nói rõ điều chế 481,25kg gang từ bao nhiêu Z không vậy bn :) ?