Xác định CTPT của anken trong các trường hợp sau:
a) Hidro hóa hoàn toàn 5,88 gam anken thu được 6,16 gam ankan tương ứng
b) Cho 3,36 gam anken tác dụng hết với dd Br2 thì tạo thành 22,56 gam sản phẩm cộng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
Đốt cháy anken luôn thu được nCO2 = nH2O
Đốt cháy ankan luôn thu được nCO2 < nH2O
=> Sự chênh lệch số mol CO2 và H2O chính là số mol của ankan.
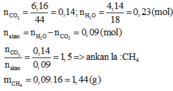

nCO2=8,96/22,4=0,4 mol
=> nC=nCO2=0,4 mol
mC=0,4.12=4,8g
=> mH=5,8-4,8=1g
nH=1 mol -> nH2O=0,5
nH=0,5 mol
Pt: CnH2n+2 + (3n+1/2)O2-> nCO2 + (n+1)H2O
0,4 0,5 mol
=> n/0,4=n+1/0,5 -> n=4
Vậy cthh cần tìm là C4H10

Vì thu được một hiđrocacbon nên ankan và anken có cùng số nguyên tử C trong phân tử là n.
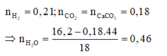
Do đó khi đốt cháy X thu được 0,18 mol CO2 và (0,46 - 0,2l) = 0,25 mol H2O
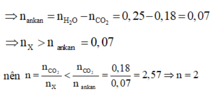
Đáp án A

Đáp án C
Đốt cháy Y cũng là đốt cháy X.
X + O2 → 0,06 mol CO2 + 0,08 mol H2O.
• nXn = H2O - nCO2 = 0,08 - 0,06 = 0,02 mol.
X có số nguyên tử C = 0,06 : 0,02 = 3; số nguyên tử H = 0,08 x 2 : 0,02 = 8 → X là C3H8.
→ hhY gồm C3H8 dư; CH4 và C2H6; mX = 0,02 x 44 = 0,88 gam.
Theo BTKL: mY = mX = 0,88 gam → nY = 0,88 : 27,5 = 0,032 mol
→ nankan phản ứng = 0,032 - 0,02 = 0,012 mol
⇒ H = 0 , 012 0 , 02 = 60 %
a)
CTPT: CnH2n
\(n_{C_nH_{2n}}=\dfrac{5,88}{14n}=\dfrac{0,42}{n}\left(mol\right)\)
PTHH: CnH2n + H2 --to,Ni--> CnH2n+2
\(\dfrac{0,42}{n}\)----------------->\(\dfrac{0,42}{n}\)
=> \(\dfrac{0,42}{n}\left(14n+2\right)=6,16\)
=> n = 3
=> CTPT: C3H6
b)
CTPT: CnH2n
\(n_{C_nH_{2n}}=\dfrac{3,36}{14n}=\dfrac{0,24}{n}\left(mol\right)\)
PTHH: CnH2n + Br2 --> CnH2nBr2
\(\dfrac{0,24}{n}\)------------>\(\dfrac{0,24}{n}\)
=> \(\dfrac{0,24}{n}\left(14n+160\right)=22,56\)
=> n = 2
=> CTPT: C2H4
Mình thiếu câu C bạn ơi
c) Hidrat hóa anken A thu được chất B, trong B có chứa 34,78% oxi về khối lượng