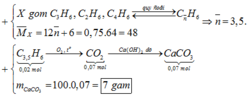
Hỗn hợp ankan X có tỉ khối hơi so với He bằng 9,25. Đốt cháy hoàn toàn 7,4g hỗn hợp X thì thu được CO2 và H2O. Dẫn toàn bộ sản phẩm cháy qua dung dịch Ba(OH)2 dư thì thu được m(g) kết tủa. Khối lượng kết tủa thu được là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Quy đổi cứ 2 mol C2H4 thành 1 mol CH4 và 1 mol C3H4
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_3H_4}=b\left(mol\right)\end{matrix}\right.\)
=> 16a + 40b = 8,4
Và \(\overline{M}=\dfrac{8,4}{a+b}=14.2=28\left(g/mol\right)\)
=> a = 0,15 (mol); b = 0,15 (mol)
Bảo toàn C: nCO2 = 0,6 (mol)
=> m = 0,6.197 = 118,2 (g)
Bảo toàn H: nH2O = 0,6 (mol)
=> a = 0,6.44 + 0,6.18 = 37,2 (g)

Chọn đáp án A
Đặt số mol CO2 và H2O tạo thành lần lượt là x,y.
Sản phẩm cháy + Ba(OH)2 dư: = 197 x − 44 x + 18 y = 107 , 82 g
Sản phẩm cháy + Ca(OH)2 dư: = 100 x – 44 x + 18 y = 36 , 04 g
⇒ x = 0 , 74 y = 0 , 3
Số nguyên tử C trung bình 0 , 74 0 , 3 = 2 , 47
⇒ X,Y có 2 và 3 nguyên tử C.
Đặt số mol của chất có 2 nguyên tử C là a, chất có 3 nguyên tử C là b
⇒ a + b = 0 , 3 2 a + 3 b = 0 , 74 ⇒ a = 0 , 16 b = 0 , 14
Đặt số nguyên tử H của chất có 2 nguyên tử C là H1, chất có 3 nguyên tử C là H2
⇒ 0,16 H1 + 0,14 H2 = 2.0,3 = 0,6
⇒ H1 = 2, H2 = 2 Þ Hiđrocabon là C2H2, anđehit C3H2O (CTCT: C H ≡ C − C H O )
n H 2 = 2 a + 3 b = 0 , 74 m o l ⇒ m H 2 = 1 , 48 g

![]()
= 0,525 – 0,15 = 0,375 mol.
m↓ = 0,375.100 = 37,5 gam.
- Chọn đáp án A.

ta có :
\(\left\{{}\begin{matrix}M_{hhkhí}=0,6.29=17,4\\n_{hhkhí}=\dfrac{3,36}{22,4}=0,15\end{matrix}\right.\)
=>PP đừng chéo : \(\dfrac{n_{CH4}}{n_{C2H4}}\)=\(\dfrac{53}{7}\)
=>\(\left\{{}\begin{matrix}nCH4=0,1325\\nC2H4=0,0175\end{matrix}\right.\)
=>BTNT:
Σ n CaCO3=n CH4+2nC2H2=0,1675 mol
=>m CaCO3=0,1675.100=16,75g
\(M_X=9,25.4=37\left(\dfrac{g}{mol}\right)=14m+2\\ \Leftrightarrow m=2,5\\ n_X=\dfrac{7,4}{37}=0,2\left(mol\right)\\ \Rightarrow n_{CO_2}=n_C=2,5.n_X=2,5.0,2=0,5\left(mol\right)\\ n_{BaCO_3}=n_{CO_2}=0,5\left(mol\right)\\ \Rightarrow m_{kt}=m_{BaCO_3}=197.0,5=98,5\left(g\right)\)