Đốt cháy hoàn toàn một hidrocacbon X. Hấp thụ toàn bộ sản phâm cháy vào dung dịch Ba(OH)2 dư tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so ới dd Ba(OH)2 ban đầu. Xác định CTPT cua X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
n C = n C O 2 = n B a C O 3 = 29 , 55 197 = 0 , 15 ( m o l ) m g i ả m = m B a C O 3 - m C O 2 + m H 2 O = 19 , 35 ⇒ m C O 2 + m H 2 O = 10 , 2 g a m m H 2 O = 10 , 2 - 0 , 15 . 44 = 3 , 6 ( g a m ) ⇒ n H 2 O = 3 , 6 18 = 0 , 2 ( m o l ) ⇒ n H = 0 , 4 ( m o l ) n C : n H = 0 , 15 : 0 , 4 = 3 : 8 ⇒ C T P T : C 3 H 8
nC : nH = 0,15 : 0,4 = 3 : 8 Þ CTPT: C3H8

Chọn C
Ta có nCO2 = nBaCO3 = 29,55/197 = 0,15 mol
(CO2 + H2O) + dd Ba(OH)2dư → BaCO3↓ + dd sau phản ứng
⇒ mCO2 + mH2O = m↓ + (mdd sau pư – mdd Ba(OH)2 bđ)
⇒ 44.0,15 + mH2O = 29,55 – 19,35 ⇒ mH2O = 3,6g nH2O = 0,2 mol
Do nH2O > nCO2 X là ankan và nX = 0,2 – 0,15 = 0,05
X có số C = 0,15/0,05 = 3 ⇒ X là C3H8

Ta có nCO2 = nBaCO3 = 29,55/197 = 0,15 mol
(CO2 + H2O) + dd Ba(OH)2dư BaCO3↓ + dd sau phản ứng
mCO2 + mH2O = m↓ + (mdd sau pư – mdd Ba(OH)2 bđ)
44.0,15 + mH2O = 29,55 – 19,35 mH2O = 3,6g nH2O = 0,2 mol
Do nH2O > nCO2 =>X là ankan và nX = 0,2 – 0,15 = 0,05
X có số C = 0,15/0,05 = 3 X là C3H8 nên chọn C.

MX = 48 → nX = 0,96/48 = 0,02
Ta có:
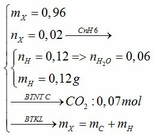
CO2 + Ba(OH)2 → BaCO3 + H2O
0,05 ←0,05 → 0,05
CO2 + BaCO3 + H2O → Ba(HCO3)2
0,02→ 0,02
Dư: 0,03
→ nBaCO3 dư = 0,03 → x = 5,91 (g) và mdd giảm = mBaCO3 – mCO2 + mH2O= 1,75 (g)
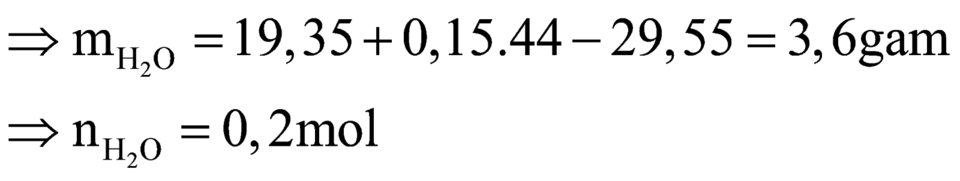
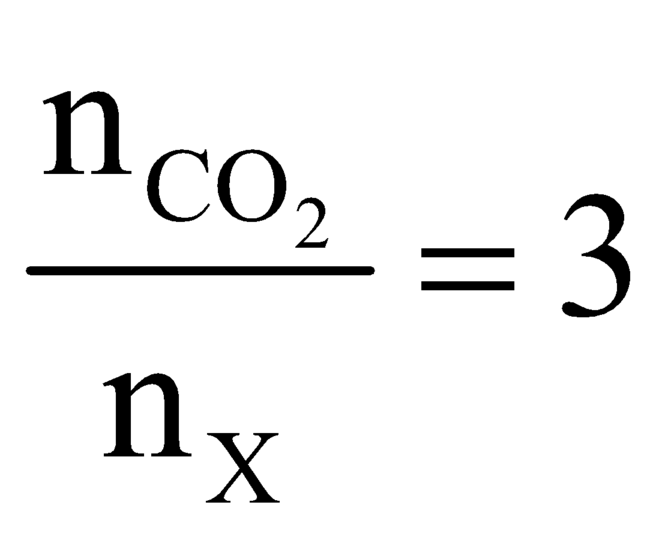

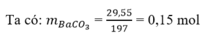
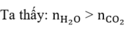
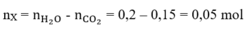
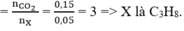
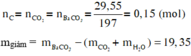
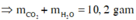
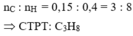
Ta có: \(n_{CO_2}=n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
m giảm = m kết tủa - mCO2 - mH2O
⇒ mH2O = 29,55 - 0,15.44 - 19,35 = 3,6 (g)
\(\Rightarrow n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Vì: Đốt cháy hiđrocacbon X thu được nH2O > nCO2 nên X là ankan.
⇒ nX = 0,2 - 0,15 = 0,05 (mol)
Gọi CTPT của X là CnH2n+2 (n ≥ 1)
\(\Rightarrow n=\dfrac{0,15}{0,05}=3\left(tm\right)\)
Vậy: X là C3H8.
Bạn tham khảo nhé!