giải bằng pthh, không dùng pt ion: Hấp thụ hết V lít CO2 vào 200 ml dung dịch hỗn hợp gồm NaOH 1M và Ba(OH)2 0,5 M, sau khi phản ứng xảy ra hoàn toàn thu được 11,82 gam kết tủa, Tính giá trị của V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{NaOH}=2.0,03=0,06\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=2.0,02=0,04\left(mol\right)\)
\(n_{CaCO3}=\dfrac{3}{100}=0,03\left(mol\right)\)
Thứ tự các pthh :
\(C+O_2-t^o->CO_2\) (1)
\(CO_2+Ca\left(OH\right)_2-->CaCO_3+H_2O\) (2)
\(CO_2+2NaOH-->Na_2CO_3+H_2O\) (3)
\(CO_2+Na_2CO_3-->2NaHCO_3\) (4)
\(CO_2+CaCO_3-->Ca\left(HCO_3\right)_2\) (5)
Vì \(n_{CaCO3}< n_{Ca\left(OH\right)2}\left(0,03< 0,04\right)\) => Có 2 giá trị của CO2 thỏa mãn
TH1: CO2 thiếu ở pứ 2 => Chỉ xảy ra pứ (1) và (2) => Không có pứ hòa tan kết tủa
Theo pthh (2) : \(n_{CO_2}=n_{CaCO3}=0,03\left(mol\right)\)
Bảo toản C : \(n_C=n_{CO2}=0,03\left(mol\right)\)
=> m = 0,03.12 = 0,36 (g)
TH2 : CO2 dư ở pứ (2) ; (3); (4), đến pứ (5) thì thiếu => Có pứ hòa tan kết tủa
Xét pứ (2); (3); (4) ; (5) :
\(\Sigma n_{CO2}=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+n_{Na2CO3}+n_{CaCO3\left(tan\right)}\)
\(=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+\dfrac{1}{2}n_{NaOH}+\left(n_{CaCO3\left(sinh.ra\right)}-n_{CaCO3thu.duoc}\right)\)
\(=n_{Ca\left(OH\right)2}+n_{NaOH}+\left(n_{Ca\left(OH\right)2}-0,03\right)\)
\(=2n_{Ca\left(OH\right)2}+n_{NaOH}-0,03\)
\(=2.0,04+0,06-0,03\)
\(=0,09\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,09\left(mol\right)\)
\(\Rightarrow m=0,09.12=1,08\left(g\right)\)
Em làm đúng rồi đấy nhưng TH 2 bước cuối chắc tính nhầm kìa nCO2 = 0,11 mol , e sửa lại nhé.

Ta có: \(n_{K_2CO_3}=0,1.0,2=0,02\left(mol\right)\)
\(n_{KOH}=0,1.1,4=0,14\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{11,82}{197}=0,06\left(mol\right)\)
TH1: KOH dư.
Giả sử: nCO2 = x (mol)
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
x_________________x (mol)
⇒ ΣnK2CO3 = x + 0,02 (mol)
\(K_2CO_3+BaCl_2\rightarrow2KCl+BaCO_3\)
x + 0,02___________________x + 0,02 (mol)
⇒ x + 0,02 = 0,06 ⇔ x = 0,04 (mol)
⇒ VCO2 = 0,04.22,4 = 0,896 (l)
TH2: KOH hết.
\(BaCl_2+K_2CO_3\rightarrow2KCl+BaCO_3\)
_________0,06_____________0,06 (mol)
⇒ nK2CO3 (do CO2 pư tạo thành) = 0,06 - 0,02 = 0,04 (mol)
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,04___0,08_______0,04 (mol)
\(CO_2+KOH\rightarrow KHCO_3\)
0,06__(0,14-0,08) (mol)
⇒ nCO2 = 0,04 + 0,06 = 0,1 (mol)
⇒ VCO2 = 0,1.22,4 = 2,24 (l)
Bạn tham khảo nhé!

Đáp án B
Do dd M và dd N đều tác dụng với KHSO4 sinh ra kết tủa nên dd M và dd N đều chứa Ba(HCO3)2


Đáp án B
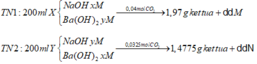
Coi phản ứng của 0,04 mol CO2 với dung dịch X là thí nghiệm 1 (TN1); phản ứng của Y với 0,0325 mol CO2 là thí nghiệm 2 (TN2).
Ở cả hai TN n BaCO 3 < n CO 2 . Mặt khác, dung dịch sau phản ứng ở hai TN phản ứng với KHSO4 đều tạo ra kết tủa. Suy ra : Dung dịch sau phản ứng còn chứa Ba2+. Ion CO 3 2 - tạo ra đã chuyển hết vào BaCO3. Dung dịch sau các phản ứng chứa
![]()
Sử dụng bảo toàn nguyên tố Ba, C và bảo toàn điện tích cho dung dịch sau phản ứng, ta có:
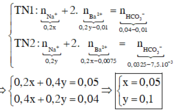

Đáp án B
M hoặc N + KHSO4 → ↓ trắng ⇒ có chứa Ba2+ ⇒ CO32– không đủ kết tủa hết Ba2+.
Mặt khác: nCO2 > nBaCO3 ở cả 2 thí nghiệm ⇒ sinh cả HCO3– và CO32–.
► Khi đó ta có công thức: nCO32– = nOH– – nCO2. ||⇒ áp dụng:
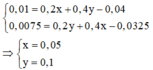

200 ml dd X có mol OH- = 0,2(x+2y) và 200 ml dd Y có mol OH- = 0,2(y + 2x) TH 1: 0,04 mol CO2 + 200 ml dd X cho 0,01 mol BaCO3 + dd M
TH 2: 0,0325 mol CO2 + 200 ml dd Y cho 0,0075 mol BaCO3 + dd N
dd M + KHSO4 và dd N + KHSO4 đều cho kết tủa ==> trong M và N có
Ba(HCO3)2 ==> CO32- hếtTH1 : mol BaCO3 = mol OH- - mol CO2 = 0,2(x+2y) - 0,04 = 0,01 ==> x
+ 2y = 0,25
TH2 : mol BaCO3 = mol OH- - mol CO2 = 0,2(2x+y) - 0,0325 = 0,0075
=> 2x + y = 0,2=> x = 0,05 và y = 0,1
=> Đáp án B



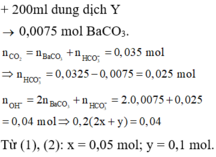
$n_{NaOH} = 0,2.1 = 0,2(mol) ; n_{Ba(OH)_2} = 0,2.0,5 = 0,1(mol)$
$n_{BaCO_3} = \dfrac{11,82}{197} = 0,06(mol)$
Thứ tự phản ứng là : (từ trên xuống dưới)
\(CO_2+Ba\left(OH\right)_2\text{→}BaCO_3+H_2O\)
0,1 0,1 0,1 (mol)
$\Rightarrow n_{BaCO_3\ bị\ hòa\ tan} = 0,1 - 0,06 = 0,04(mol)$
\(2NaOH+CO_2\text{→}Na_2CO_3+H_2O\)
0,2 0,1 0,1 (mol)
\(Na_2CO_3+CO_2+H_2O\text{→}2NaHCO_3\)
0,1 0,1 (mol)
\(BaCO_3+CO_2+H_2O\text{→}Ba\left(HCO_3\right)_2\)
0,04 0,04 (mol)
Suy ra: $n_{CO_2} = 0,1 + 0,1 + 0,1 + 0,04 = 0,34(mol)$
$V = 0,34.22,4 = 7,616(lít)$
\(\left\{{}\begin{matrix}n_{NaOH}=1.0,2=0,2\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3}=\dfrac{11,82}{197}=0,06\left(mol\right)\)
TH1: Kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
_____________0,06<------0,06
=> VCO2 = 0,06.22,4 = 1,344(l)
TH2: Kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
_______0,1----->0,1------->0,1
2NaOH + CO2 --> Na2CO3 + H2O
_0,2---->0,1------->0,1
Na2CO3 + CO2 + H2O --> 2NaHCO3
_0,1----->0,1
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,04--->0,04
=> nCO2 = 0,34 (mol)
=> VCO2 = 0,34.22,4 = 7,616(l)