Tìm thể tích của hỗ hợp khí( đktc) gồm có: 3,4g khí H2S và 0,3.1023 phân tử khí SO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


V C O 2 = n C O 2 . 22,4 = 0,25.22,4 = 5,6 (l)
V O 2 = n O 2 .22,4 = 0,25.22,4 = 5,6 (l)
n
N
2
=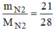 = 0,75(mol)
= 0,75(mol)
→ V N 2 = n N 2 .22,4 = 0,75.22,4= 16,8 (l)
n
C
O
2
=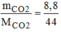 = 0,2 (mol)
= 0,2 (mol)
→ V C O 2 = n C O 2 . 22,4 = 0,2.22,4 = 4,48 (l)
n
H
2
=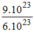 =1,5(mol)
=1,5(mol)
→ V H 2 = n H 2 . 22,4 = 1,5. 22,4 = 33,6 (l)
n
C
O
=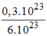 = 0,05(mol)
= 0,05(mol)
→ V C O = n C O . 22,4 = 0,05. 22,4 = 1,12 (l)

\(a,V_{CO_2}=0,4.22,4=8,96(l)\\ b,V_{hh}=22,4.(0,25+0,5)=16,8(l)\\ c,V_{H_2S}=0,5.22,4=11,2(l)\)

Đáp án C.
Khối lượng mol phân tử của X : 1,0625 x 32 = 34 (gam).
n SO 2 = 2,24/22,4 = 0,1 mol.
Trong 0,1 mol SO 2 có 0,1 mol nguyên tử s ứng với khối lượng : m S = 32 x 0,1 = 3,2 (gam).
n H 2 O = 1,8/18 = 0,1 mol trong đó có 0,2 mol nguyên tử H ứng với khối lượng : 1 x 0,2 = 0,2 (gam).
m X = m S + m H = 3,4g như vậy chất X không có oxi.
n X = 3,4/34 = 0,1 mol
Do đó : 0,1 mol phân tử X có chứa 0,1 moi nguyên tử S và 0,2 mol nguyên tử H.
Vậy 1 mol phân tử X có chứa 1 mol nguyên tử S và 2 mol nguyên tử H
Công thức hoá học của hợp chất X là H 2 S

Gọi hỗn là: A
* Thể tích hỗn hợp khí A là:
VA = ( 0.25 + 0.5 ) . 22,4
= 16.8 lít
* mSO3 = 0,25 . 96 = 24g
mCO = 0,5 . 28 = 14g
⇒ Khối lượng của hỗn hợp khí A là:
mA = 24g + 14g = 38g

a.
\(V_{H_2S}=0.75\cdot22.4=16.8\left(l\right)\)
\(V_{SO_2}=\dfrac{12.8}{64}\cdot22.4=4.48\left(l\right)\)
\(V_{O_2}=\dfrac{3.2}{32}\cdot22.4=2.24\left(l\right)\)
b.
\(n_{hh}=\dfrac{22}{44}+\dfrac{3.55}{71}+\dfrac{0.14}{28}=0.555\left(mol\right)\)
\(V_{hh}=0.555\cdot22.4=12.432\left(l\right)\)

\(n_{H_2}=\dfrac{12.10^{22}}{6.10^{23}}=0,2\left(mol\right)\)
\(n_{SO_2}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
=> Vhh = 0,25.22,4 + 4,48 + 0,2.22,4 + 0,05.22,4 = 15,68(l)
V\(H_2S\) = \(\left(\dfrac{3,4}{34}\right).22,4=2,24l\)
\(n_{SO_3}=\dfrac{0,3.10^{23}}{6.10^{23}}=0,05mol\)
\(\Rightarrow V_{SO_3}=0,05.22,4=1,12l\)
\(\Rightarrow V_{hh}=2,24+1,12=3,36l\)