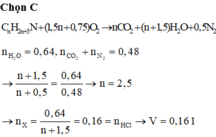Hỗn hợp khí A gồm metan và hidrocacbon. Đốt cháy hoàn toàn 1,0 lít A cần dùng vừa đủ 2,6 lít khí O2 thu được CO2 và hơi nước. Dẫn toàn bộ sản phẩm cháy lội từ từ vào dung dịch H2SO4 đặc dư thấy có 1,6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hiddrocacbon và tính phần trăm thể tích của CH4 trong hỗn hợp A. Biết rằng các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Công thức chung của este đơn chức, mạch hở, chứa một liên kết đôi C=C là C n H 2 n - 2 O 2
Phản ứng đốt cháy: C n H 2 n - 2 O 2 + 1 , 5 n - 1 , 5 O 2 → n C O 2 + n - 1 H 2 O
Dung dịch H 2 S O 4 hấp thụ H 2 O trong số các sản phẩm cháy.
Do đó m H 2 O = 2 , 25 g a m ⇒ n H 2 O = 0 , 14 m o l
Từ phản ứng cháy nhận thấy: n O 2 = 1 , 5 n H 2 O = 0 , 21 m o l ⇒ V = 4,704.

Chọn đáp án B
Cách 1: Biến đổi peptit – giải đốt cháy kết hợp thủy phân
đốt muối T dạng C n H 2 n N O 2 N a + O 2 → N a 2 C O 3 + 38,07 gam C O 2 + H 2 O + 0,1 mol N 2 .
⇒ có n T = 0,2 mol ⇒ n N a C O 3 = 0,1 mol ⇒ n C = n H 2 = (38,07 + 0,1 × 44) ÷ (44 + 18) = 0,685 mol.
⇒ m T = 0,685 × 14 + 0,2 × (46 + 23) = 23,39 gam. Quan sát lại phản ứng thủy phân:
m gam E + 0,2 mol NaOH → 23,39 gam muối T + x mol H 2 O .
đốt m gam E cho 0,63 mol H 2 O ||⇒ bảo toàn H có 2x = 0,09 mol ⇒ x = 0,045 mol.
⇒ BTKL phản ứng thủy phân có m = 0,045 × 18 + 23,39 – 0,2 × 40 = 16,20 gam → Chọn B. ♦.
Cách 2: tham khảo: tranduchoanghuy
Quy E về C 2 H 3 N O , C H 2 , H 2 O ⇒ T gồm C 2 H 3 N O 2 N a v à C H 2 .
⇒ n C 2 H 3 N O = n C 2 H 4 N O 2 N a = 2 n N 2 = 0,2 mol ⇒ n N a C O 3 = 0,1 mol.
⇒ n H 2 O = (38,07 + 0,1 × 44) ÷ (44 + 18) = 0,685 mol ⇒ n C H 2 = 0,285 mol.
Bảo toàn H có: n H 2 O trong E = (0,63 × 2 – 0,2 × 3 – 0,285 × 2) ÷ 2 = 0,045 mol.
⇒ m = 0,2 × 57 + 0,285 × 14 + 0,045 × 18 = 16,2 gam

Đáp án C
Vì các hợp chất thuộc cacbohidrat có dạng Cn(H2O)m
⇒ Khi đốt cháy các hợp chất cacbohidrat thì nO2 pứ = ∑nC = 1,68 mol.
⇒ nBaCO3 = nC = 1,68⇒ mBaCO3 = 330,96 gam.

Chọn đáp án C
Vì các hợp chất thuộc cacbohidrat có dạng Cn(H2O)m
⇒ Khi đốt cháy các hợp chất cacbohidrat thì nO2 pứ = ∑nC = 1,68 mol.
⇒ nBaCO3 = nC = 1,68⇒ mBaCO3 = 330,96 gam.

Chọn đáp án C
Vì các hợp chất thuộc cacbohidrat có dạng Cn(H2O)m
⇒ Khi đốt cháy các hợp chất cacbohidrat thì nO2 pứ = ∑nC = 1,68 mol.
⇒ nBaCO3 = nC = 1,68⇒ mBaCO3 = 330,96 gam.