Trong phương trình phản ứng : 16HCl + 2KMnO4 -> 2KCl + 5Cl2 + 2MnCl2 + 8H2O
Xác định vai trò của KMnO4? Giải thích.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tổng hệ số nguyên ( đơn giản nhất ) : $16+2+2+5+2+8=35$
=> Chọn B.

Có 2 phản ứng mà H+ đóng vai trò là chất oxi hóa: (a), (d). Đáp án A

Chọn A . Gồm:
4HCl + MnO2 → t o MnCl2 + Cl2 + 2H2O.
14HCl
→
t
o
2KCl + 2CrCl3 + 3Cl2 + 7H2O
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O

Đáp án C
HCl thể hiện tính oxi hóa bị bị khử thành H2:
![]()
Các phản ứng trong đó HCl thể hiện tính oxi hóa là:
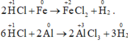

HCl thể hiện tính oxi hóa ở nguyên tố H+ xuống H2
Vậy có 2 phương trình (c), (d) HCl thể hiện tính oxi hóa. Đáp án B.

Chọn C.
Phản ứng mà HCl thể hiện tính oxi hóa nghĩa là phản ứng mà trong đó HCl có số oxi hóa giảm.

Đáp án D
Phản ứng tạo ra H2 là phản ứng mà HCl đóng vai trò là chất oxi hóa
Mn+7 +5e --> Mn+2
Do nguyên tử Mn nhận thêm e => KMnO4 đóng vai trò chất oxi hóa