Bài 13. Đốt cháy 4,6 gam Natri trong bình chứa khí Clo .
a) Tính thể tích khí Clo ở đktc
b) Tính khối lượng NaCl thu được, biết hiệu suất phản ứng đạt 80%
c)LấylượngNaClthuđượcởtrênhòatanvàonướcthuđược500gamdungdịch muối. Tính C% dung dịch muối này
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=\dfrac{1,08}{27}=0,04\left(mol\right)\\ 2Al+3Cl_2\rightarrow\left(t^o\right)2AlCl_3\\ a,n_{Cl_2}=\dfrac{3}{2}.0,04=0,06\left(mol\right)\\ V_{Cl_2\left(\text{Đ}KTC\right)}=0,06.22,4=1,344\left(l\right)\\ b,C1:m_{AlCl_3}=m_{Al}+m_{Cl_2}=1,08+71.0,06=5,34\left(g\right)\\ C2:n_{AlCl_3}=n_{Al}=0,04\left(mol\right)\\ m_{AlCl_3}=0,04.133,5=5,34\left(g\right)\)

\(n_{Al}=\frac{1,08}{27}=0,04mol\)
\(2Al+3Cl_2\rightarrow^{t^o}2AlCl_3\)
a) \(n_{Cl_2}=\frac{3}{2}.0,04=0,06mol\)
\(V_{Cl_2}=0,06.22,4=1,344l\)
b) Cách 1: \(m_{AlCl_3}=m_{Al}+m_{Cl_2}=1,08+71.0,06=5,34g\)
Cách 2: \(n_{AlCl_3}=n_{Al}=0,04mol\)
\(m_{AlCl_3}=0,04.133,5=5,34g\)

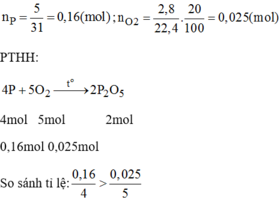
Vậy P dư nen tính bài toán theo n O 2
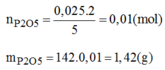
Khối lượng P 2 O 5 thực tế thu được: 1,42.80% = 1,136(g)

P/ứng hóa học: \(Mg+Cl_2->MgCl_2\)
Công thức của p/ứng có phải CT về khối lượng không nhỉ? Mình chưa hiểu lắm. Nếu là CT về kh lượng thì:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
* Khối lượng khí clo đã p/ứ:
Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\\ =>12g+m_{Cl_2}=47,5g\\ =>m_{Cl_2}=47,5g-12g=35,5g\)
Vậy có 35,5g khí Clo tham gia p/ứng.

Ta có: \(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
PT: \(2Na+Cl_2\rightarrow2NaCl\)
____0,1___0,05____0,1 (mol)
a, mNa = 0,1.23 = 2,3 (g)
b, VCl2 = 0,05.22,4 = 1,12 (l)
Bạn tham khảo nhé!

TL
PTHH : 2R + nCl2 --> 2RCln (n là hoá trị của R)
Áp dụng định luật bảo toàn khối lượng: mCl2 = 53,4 - 10,8 = 42,6 (g)
=> nCl2 = 42,6 : 71 = 0,6 (mol)
Áp dụng công thức: n = \({P . V \over R . T}\)
=>VCl2 (20o , 0,75 atm) = 19,2208 (l)
Khi nào rảnh vào kênh H-EDITOR xem vid nha!!! Thanks!

