Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chỉ có HCl tác dụng với MnO2 ở nhiệt độ thường mới điều chế được khí Clo.
Các cặp chất khác đều có nhiệt độ cao.

-Thí nghiệm: Cho một ít KMnO4 hoặc KClO3 vào ống nghiệm có cắm ống dẫn khí,đầu ống nghiệm được nút lại.
Câu hỏi là: cách điều chế oxi trong phòng thí nghiệm á
Giúp mình đi mọi ngừi ơiii 😥🥺


a. Khí O2 ít tan trong nước và nặng hơn không khí nên cách 1b không được (khi đó không khí sẽ xua hết khí O2 ra ngoài), trong phòng thí nghiệm người ta sử dụng cách 1a
b. Điều chế khí O2 người ta nhiệt phân các hợp chất giàu oxi: KMnO4; KClO3
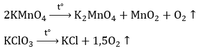

a)
Nung các hợp chất giàu O2 như KMnO4 , KClO3 , ....
b)
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
a, - Thường được điều chế bằng cách nung nóng KMnO4 .
b, PTHH : 2KMnO4 -> K2MnO4 + MnO2 + O2

Chọn C
Trong phòng thí nghiệm, oxi được điều chế bằng cách phân hủy các hợp chất giàu oxi, kém bền với nhiệt như KMnO 4 ; KClO 3 …
![]()

Chọn C
Trong phòng thí nghiệm, oxi được điều chế bằng cách phân hủy các hợp chất giàu oxi, kém bền với nhiệt như K M n O 4 , K C l O 3 …
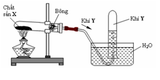
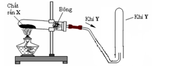

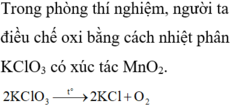
Trong phòng thí nghiệm, người ta điều chế khí oxi bằng cách nhiệt phân KClO₃ hay KMnO₄ vì giàu oxi và dễ phân hủy tạo ra oxi
Nhiệt phân \(KMnO_4,KClO_3 :\)
\(2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ 2KClO_3 \xrightarrow{t^o,MnO_2} 2KCl + 3O_2\)