cho 5,4 g một kim loại R( có hóa trị từ 1 đến 3) tác dụng vừa đủ với dung dịch h2so4 loãng dư thu được 34,2 (g) muối. xác định kim loại R
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{R_2O}=\dfrac{18,6}{2M_R+16}\left(mol\right);n_{RCl}=\dfrac{35,1}{M_R+35,5}\left(mol\right)\)
PTHH: R2O + 2HCl ---> 2RCl + H2O
Theo PT: \(2n_{R_2O}=n_{RCl}\)
=> \(\dfrac{2.18,6}{2M_R+16}=\dfrac{35,1}{M_R+35,5}\)
=> MR = 23 (g/mol)
=> R là Natri (Na)
=> Oxide là Na2O
\(R_2O+2HCl\rightarrow2RCl+H_2O\\ n_{Cl}=n_{HCl}=\dfrac{35,1-18,6}{71-16}=0,3\left(mol\right)\\ n_{oxit}=\dfrac{n_{HCl}}{2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ M_{oxit}=\dfrac{18,6}{0,15}=124\left(\dfrac{g}{mol}\right)=2M_R+M_O\\ \Leftrightarrow2M_R+16=124\\ \Leftrightarrow M_R=54\left(\dfrac{g}{mol}\right)\)
Em xem lại đề

\(n_{H2\left(dktc\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,2 0,3
\(n_R=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\left(dvc\right)\)
Vậy kim loại R là nhôm
b) \(2Al+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(n_{SO2}=\dfrac{0,3.3}{2}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
Chúc bạn học tốt
a) PTHH: \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_R=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) R là Nhôm (Al)
b) PTHH: \(2Al+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
Theo PTHH: \(n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,3\cdot22,4=6,72\left(l\right)\)

Xét 1 mol kim loại ứng với R (gam) tham gia phản ứng.
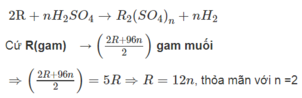
Vậy R=24 (Mg)

R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)

\(n_A=\dfrac{5,4}{M_A}\left(mol\right)\)
PTHH: 2A + 3Cl2 --to--> 2ACl3
_____\(\dfrac{5,4}{M_A}\)-------------->\(\dfrac{5,4}{M_A}\)
=> \(\dfrac{5,4}{M_A}\left(M_A+35,5.3\right)=26,7=>M_A=27\left(Al\right)\)
Gọi kim loại là \(R\)
Ta có phương trình:
\(2R+3Cl_2\rightarrow2RCl_3\)
M---------------------M+106,5
5,4-----------------------26,7
Áp dụng tam suất => 26,7M=5,4M+575,1 <=> M=27
=> \(R\) là nhôm \(\left(Al\right)\)
Gọi hóa trị của R là n
PTHH : \(2R+nH_2SO_4-->R_2\left(SO_4\right)n+nH_2\)
Theo pthh : \(n_{R2\left(SO4\right)n}=\dfrac{1}{2}n_R\)
\(\Rightarrow\dfrac{34,2}{2M_R+96n}=\dfrac{1}{2}.\dfrac{5,4}{M_R}\)
\(\Rightarrow M_R=9n\)
Ta có bảng sau :
Al
Vậy R là kim loại Al