Cho 8,64g hỗn hợp A gồm 2 kim loại là Al và Cu tác dụng vừa đủ với V ml dung dịch axit HCl 1M thu được 6,72 khí X đktc.
a)Viết PTHH xác định khí X b)Tính thành phần % về khối lượng các kim loại trong A c) Tính V giúp mình với các bạn ơi! cần gấp trong tối nay! mình cảm ơn!Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, 24nMg + 27nAl = 6,12 (1)
Theo PT: \(n_{H_2}=n_{Mg}+\dfrac{3}{2}n_{Al}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,12\left(mol\right)\\n_{Al}=0,12\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,12.24}{6,12}.100\%\approx47,06\%\\\%m_{Al}\approx52,94\%\end{matrix}\right.\)

Gọi số mol Al, Fe là a, b (mol)
=> 27a + 56b = 11,1 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Fe + 2HCl --> FeCl2 + H2
b------------------------>b
=> 1,5a + b = 0,3 (2)
(1)(2) => a = 0,1; b = 0,15
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{11,1}.100\%=24,32\%\\\%m_{Fe}=\dfrac{0,15.56}{11,1}.100\%=75,68\end{matrix}\right.\)

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a_______a_______a_____a (mol)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
2b______3b__________b_____3b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27\cdot2b=11\\a+3b=0,2\cdot2=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1\cdot56}{11}\cdot100\%\approx50,91\%\\\%m_{Al}=49,09\%\end{matrix}\right.\)
Theo các PTHH: \(\left\{{}\begin{matrix}n_{H_2}=0,4\left(mol\right)\\n_{FeSO_4}=0,1\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,4\cdot22,4=8,96\left(l\right)\\C_{M_{FeSO_4}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\\C_{M_{Al_2\left(SO_4\right)_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)
a) nH2SO4=0,4(mol)
Đặt: nFe=x(mol); nAl=y(mol) (x,y>0)
PTHH: Fe + H2SO4 -> FeSO4 + H2
x________x______x______x(mol)
2Al + 3 H2SO4 -> Al2(SO4)3 + 3 H2
y____1,5y_______0,5y_______1,5y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}56x+27y=11\\x+1,5y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> mFe=0,1.56=5,6(g)
=>%mFe=(5,6/11).100=50,909%
=>%mAl= 49,091%
b) V(H2,đktc)=0,4.22,4=8,96(l)
c) nAl2(SO4)3= 0,5y=0,5.0,2=0,1(mol)
nFeSO4=x=0,1(mol)
Vddsau=VddH2SO4=0,2(l)
=>CMddAl2(SO4)3= 0,1/0,2=0,5(M)
CMddFeSO4=0,1/0,2=0,5(M)

Một bếp lửa chờn vờn sương sớm
Một bếp lửa ấp iu nồng đượm
Cháu thương bà biết mấy nắng mưa
Hình ảnh “bếp lửa” trong màn sương sớm đã được khắc họa giản dị nhưng rõ nét và sống động qua ba câu thơ. “Bếp lửa” có lúc sáng mãnh liệt, có lúc yếu, không định hình đã trở thành một đồ dùng, một hình ảnh gần gũi và quen thuộc trong cuộc sống hằng ngày của người dân Việt Nam. Đó không chỉ là nơi để đun nấu mà còn là nơi sum họp, ghi dấu những niềm vui, nỗi buồn của mọi gia đình. Điệp ngữ “một bếp lửa” cùng với các từ láy “chờn vờn”, “ấp iu” đã gợi nên sự ấm áp, đầy tình thương yêu như tấm lòng bà. Từ “ấp iu” gợi lên sự khéo léo của bàn tay bà khi bà nhóm bếp lửa, tấm lòng yêu thương, chi chút của bà đến con cháu. Trong hồi tưởng của cháu, hình ảnh người bà luôn hiện diện cùng bếp lửa qua bao năm tháng. Hình ảnh của bà hiện lên một cách nhẹ nhàng nhưng vô cùng đẹp đẽ trong trái tim người cháu, bà vẫn luôn nhóm bếp lửa mỗi sáng mỗi chiều suốt cả cuộc đời. Hình ảnh “bếp lửa” là biểu hiện cụ thể và sinh động về sự tần tảo, chăm sóc và yêu thương của người bà đối với con cháu trong mọi hoàn cảnh khó khăn, gian khổ. Trước sự hy sinh của bà, người cháu luôn “thương bà biết mấy nắng mưa”. Từ đó làm bật lên tình cảm sâu nặng của người cháu một cách thật tự nhiên, không thể tà xiết vì những “nắng mưa”, khó nhọc vất vả của cuộc đời bà. Từ “thương” diễn đạt rất chân thật mà giản dị không chút hoa mỹ tấm lòng yêu mến bà của cháu.

\(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Fe + H2SO4 → FeSO4 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Gọi x,y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=11\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=>\(\%m_{Fe}=\dfrac{0,1.56}{11}.100=50,91\%\)
=> %m Al = 100 - 50,91 =49,09 %
b)Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,4\left(mol\right)\)
=> \(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c) \(CM_{FeSO_4}=\dfrac{0,1}{0,2}=0,5M\)
\(CM_{Al_2\left(SO_4\right)_3}=\dfrac{\dfrac{0,2}{2}}{0,2}=0,5M\)

a)
$Cu + 4HNO_3 \to Cu(NO_3)_2 + 2NO_2 + 2H_2O$
$Ag + 2HNO_3 \to AgNO_3 + NO_2 + H_2O$
b)
Gọi $n_{Cu} = a(mol) ; n_{Ag} = b(mol) \Rightarrow 64a + 108b = 4,52(1)$
$n_{NO_2} =2a + b = 0,07(2)$
Từ (1)(2) suy ra a = 0,02 ; b = 0,03
$\%m_{Cu} = \dfrac{0,02.64}{4,52}.100\% = 28,31\%$
$\%m_{Ag} = 71,69\%$

\(n_{HCl}=0,3.1=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,3 0,15 ( mol )
\(m_{Al}=0,1.27=2,7g\)
\(\Rightarrow m_{Al}=9,1.2,7=6,4g\)
\(V_{H_2}=0,15.22,4=3,36l\)
nHCl = 0,3 . 1 = 0,3 (mol)
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Mol: 0,1 <--- 0,3 ---> 0,1 ---> 0,15
mAl = 0,1 . 27 = 2,7 (g(
mCu = 9,1 - 2,7 = 6,4 (g)
VH2 = 0,15 . 22,4 = 3,36 (l)

1)
Fe + 2HCl --> FeCl2 + H2
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
2)
- Xét TN1:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<------------------0,15
=> mFe = 0,15.56 = 8,4 (g)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{8,4}{14,8}.100\%=56,757\%\\\%m_{Cu}=100\%-56,757\%=43,243\%\end{matrix}\right.\)
3)
- Xét TN2:
\(n_{Cu}=\dfrac{29,6.43,243\%}{64}=0,2\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,2-------------------------->0,2
=> V = 0,2.22,4 = 4,48 (l)
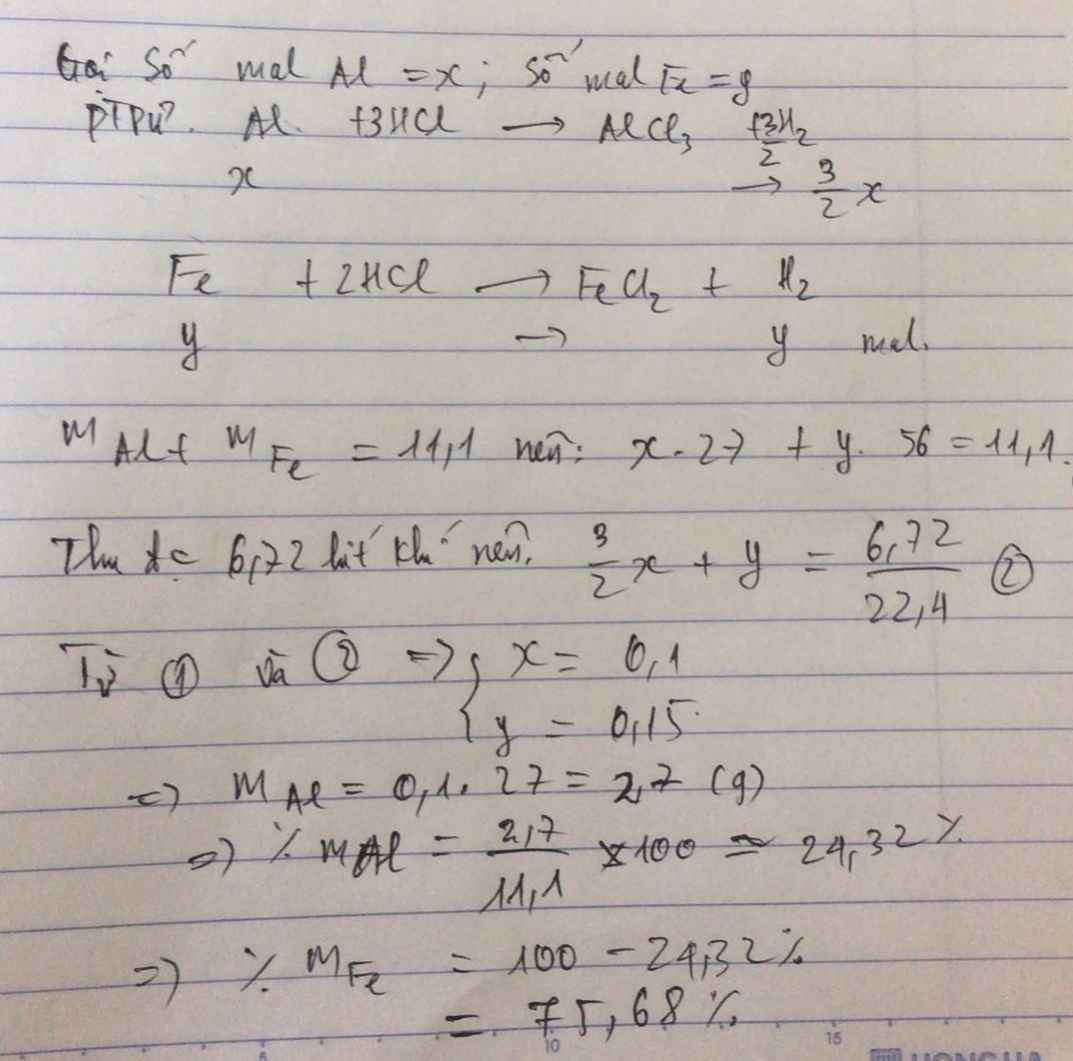


a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
X là khí Hidro
b) Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_{Al}=0,2mol\)
\(\Rightarrow\%m_{Al}=\dfrac{0,2\cdot27}{8,64}\cdot100\%=62,5\%\) \(\Rightarrow\%m_{Cu}=37,5\%\)
c) Theo PTHH: \(n_{HCl}=3n_{Al}=0,6mol\)
\(\Rightarrow V_{HCl}=\dfrac{0,6}{1}=0,6\left(l\right)=600\left(ml\right)\)