Cho 46,8 gam hỗn hợp CuO và Fe3O4 (tỉ lệ mol 1: 1) tan hết trong dung dịch H2SO4 loãng, vừa đủ, thu được dung dịch A. Cho m gam Mg vào A, sau khi phản ứng kết thúc thu được dung dịch B. Thêm dung dịch KOH dư vào B được kết tủa D. Nung D trong không khí đến khối lượng không đổi, thu được 45,0 gam chất rắn E. Giá trị gần nhất của m là
A. 8,8
B. 11,0
C. 6,6
D. 13,2


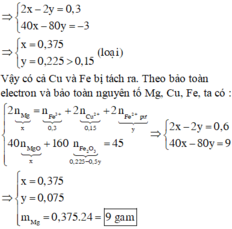



Đáp án A
Ta có số mol CuO và Fe3O4 là 0,15 mol.
Cho lượng trên tan hết trong H2SO4 thu được dung dịch A chứa CuSO4 0,15 mol, FeSO4 0,15 mol và Fe2(SO4)3 0,15 mol.
Gọi số mol của Mg là x mol.
Cho Mg vào A ta có các trường hợp sau:
+Mg chỉ tác dụng với Fe2(SO4)3 thì lúc này rắn E chứa CuO 0,15 mol , MgO x mol và Fe2O3 .
Giải được x>0,225 vô lý (loại).
+Mg tác dụng với CuSO4 lúc này rắn E chứa Fe2O3 0,225 mol, MgO x mol và CuO 0,3-x mol.
Giải được x=0,375 >0,3 vô lý (loại).
+Mg tác dụng với FeSO4 lúc này rắn E chứa MgO x mol và Fe2O3
Giải được x=0,375 mol → m = 9 gam.