Khi nhiệt độ tăng thêm 100C, tốc độ của phản ứng hóa học tăng lên bốn lần. Hỏi tốc độ phản ứng đó sẽ giảm đi bao nhiêu lần khi nhiệt độ giảm từ 700C xuống 400C
A. 44 lần
B. 64 lần
C. 54 lần
D. 24 lần
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

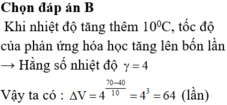

Chọn đáp án C
Cứ tăng lên 100C thì tốc độ tăng 2 lần
Vậy tăng 10.k0C thì vận tốc tăng 2k lần
k=8 ∆ v = 2 8 = 256 (lần)

Đáp án D
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 10°C chính là hệ số nhiệt độ g
Suy ra g = 3.
Thay vào công thức ta có tỉ số tốc độ phản ứng:
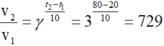
Vậy tốc độ phản ứng tăng 729 lần khi nhiệt độ tăng từ 20°C tới 80°C.

Đáp án D
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 10°C chính là hệ số nhiệt độ g
Suy ra g = 3.
Thay vào công thức ta có tỉ số tốc độ phản ứng:

Vậy tốc độ phản ứng tăng 729 lần khi nhiệt độ tăng từ 20°C tới 80°C.

Đáp án B
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 100C chính là hệ số nhiệt độ γ.
Suy ra γ = 3.
Gọi nhiệt độ sau khi tăng là t2
Thay vào công thức ta có
81 = 3 ( 1 - 30 ) / 10 ⇔ ( t 2 - 30 ) 10 = 4 ⇔ t 2 = 70 0 C

Đáp án B
Theo định nghĩa, số lần tăng tốc độ phản ứng khi nhiệt độ thay đổi 100C chính là hệ số nhiệt độ γ.
Suy ra γ = 3.
Gọi nhiệt độ sau khi tăng là t2
Thay vào công thức ta có
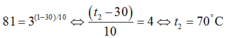

Đáp án C
Tốc độ phản ứng tức thời: v = k[H2]3.[N2]
Vậy khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên 23 = 8 lần.