Hòa tan hết m gam P2O5 vào 400 gam dung dịch KOH 10% dư sau phản ứng hoàn toàn cô cạn dung dịch thu được 3,5m gam chất rắn. Giá trị nào sau đây gần nhất với giá trị m ?
A. 14,00
B. 16,00
C. 13,00
D. 15,00
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nKOH = (400.10%)/(100%.56) = 5/7 (mol)
Gọi nP2O5 = x (mol) => nH3PO4 = 2x (mol)
KOH dư nên muối thu được là K3PO4 : 2x (mol)
Gọi nKOH dư là y (mol)
Ta có: 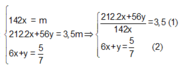
Thế (2) vào (1) => x = 0,09779 => mP2O5 = 142. 0,9779 = 13,88 (gam) ≈ 14(gam)

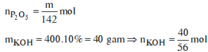
Có thể coi P2O5 tác dụng với H2O trong dung dịch KOH sinh ra H3PO4, sau đó H3PO4 tác dụng với KOH:
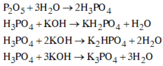
![]()
![]()
*Trường hợp 1: KOH hết
![]()
![]()
![]()
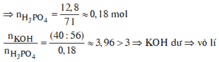
Phương trình hóa học:
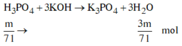
Phương trình hóa học: 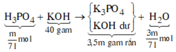
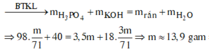
![]()
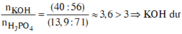
=> thỏa mãn
M=13,9 gam gần 14 gan nhất. Đáp án A.

Chọn D.
Ta có: ![]()
Chất rắn gồm NaCl (0,1); Na2SO4 (0,05); NaOH (0,4) Þ m = 28,95 gam.

Na tác dụng với axit trước.
Dung dịch sau phản ứng gồm: Na+; Cl-; SO42-
⟶m = 28,952
Đáp án D
Chọn đáp án A