Một bình kín chứa N = 3 , 01 . 10 23 phân tử khí heli.
a/ Tính khối lượng khí Heli chứa trong bình.
b/ Biết nhiệt độ khí là 0 ∘ C và áp suất khí trong bình là 1atm ( 1 , 013 . 10 5 Pa). Hỏi thể tích của bình là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1/ Bạn phải biết số A vô ga đrô = \(6,023.10^{23}\) hạt.
a/ nHe = \(3,01.10^{23}\text{/}6.0,23.10^{23}=0,5\) (mol) => mHe = \(0,5.4=2\) (g)
b/ V = \(0,5.22,4=11,2\left(l\right)\)
cho mình hỏi cái , kêu tính thể tích bình , cho nên khi bao lõi thành bình nên thể tich khí heli = thể tích bình hả bạn

a)Áp dụng quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\)
\(\Rightarrow\dfrac{p_1}{p_2}=\dfrac{27+273}{177+273}=\dfrac{2}{3}\)
\(\Rightarrow p_2=\dfrac{2}{3}p_1=\dfrac{2}{3}p\)

Đáp án: C
Ta có:
- Ban đầu, khí Heli có khối lượng m, thể tích V, áp suất p, nhiệt độ T1
PT: p 1 V = m M R T 1 1
- Sau một thời gian, khí Heli có khối lượng m′, thể tích V, áp suất p2, nhiệt độ T2
PT: p 2 V = m ' M R T 2 2
Lấy 2 1 ta được: p 2 p 1 = m ' m T 2 T 1
Trừ cả hai vế cho 1, ta đươc:
p 2 p 1 − 1 = m ' m T 2 T 1 − 1 ↔ p 2 − p 1 p 1 = m ' T 2 − m T 1 m T 1 = m ' T 2 + Δ T − m T 1 m T 1 ↔ Δ p p 1 = m ' − m m + m ' m Δ T T 1 3
Mặt khác, theo đề bài, ta có: Δ p p 1 = − 0,2 Δ T T 1 = − 0,1
Thế vào (3), ta được:
− 0,2 = m ' − m m + m ' m − 0,1 ↔ m ' − m − 0,1 m ' = − 0,2 m ↔ 0,9 m ' = 0,8 m → m ' = 8 9 m
=> Lượng khí Heli đã thoát ra:
Δ m = m − m ' = m − 8 9 m = m 9 = 0,3 9 = 0,03333 k g = 33,33 g

Chọn B.
Ban đầu, lúc chưa làm thoát khí ta có:
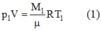
Khi làm thoát khí, lượng khí còn lại trong bình là
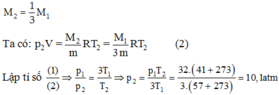

Chọn D.
Áp dụng phương trình Cla-pê-rôn – Men-đê-lê-ép:
+ Trạng thái 1 (khi chưa tăng nhiệt độ):
Khối lượng m1, p1 = 5.105 Pa, V1 = 4,8 lít, T1 = 287 K
Từ phương trình:
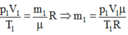
+ Trạng thái 2 (khi đã tăng nhiệt độ):
Khối lượng m2, p2 = p1 = 5.105 Pa, V2 = V1 = 4,8 lít, T2 = 26 + 273 = 287 K.
Từ phương trình:
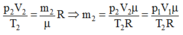
Khối lượng khí thoát ra ngoài:
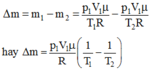
Thay số:
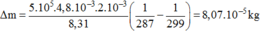

Trạng thái 1: \(\left\{{}\begin{matrix}p_1=10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=5\cdot10^5Pa\\T_2=???\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{10^5}{300}=\dfrac{5\cdot10^5}{T_2}\)
\(\Rightarrow T_2=1500K=1227^oC\)

Xét lượng khí trong bình.
Trạng thái đầu: V 1 = 8 lít; T 1 = 100 + 273 = 373 K ; p 1 = 10 5 N/ m 2
Trạng thái cuối: V 2 = 8 lít; T 2 = 20 + 273 = 293 K; p 2 = ?
Vì thể tích không đổi nên:
p 1 / T 1 = p 2 / T 2 ⇒ p 2 = p 1 T 2 / T 1 = 7,86. 10 4 N/ m 2
a)
Cứ N A phân tử (nguyên tử) He có khối lượng 4g.
Chú ý: N = 3 , 01.10 23 = N A 2
⇒ khối lượng He trong bình: m = 4 2 = 2 g
b)
Trong điều kiện nhiệt độ và áp suất như trên (ĐKTC),
thể tích của 1 mol He là V 0 = 22,1 lít. Vì lượng khí He
trong bình chỉ là 0,5 mol nên thể tích của bình là:
V = V 0 2 = 11 , 2 lít.