Đốt cháy hoàn toàn 0,8 mol hỗn hợp gồm đimetyl ete và ancol etylic ở trạng thái hơi, cho toàn bộ sản phẩm qua dung dịch Ca(OH)2 dư. Vậy khối lượng kết tủa thu được là:
A. 80g
B. 160g
C. 170g
D. 150g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Hướng dẫn
Cả 2 chất trên đều có công thức phân tử là C2H6O.
Khi đốt cháy C2H6O → 2CO2
=> số mol CO2 = 0,8.2 = 1,6 mol.
CO2 + Ca(OH)2 → CaCO3 + H2O
=> Khối lượng kết tủa = 1,6.100 = 160 (gam)

Các chất trong hỗn hợp đều chứa 2 liên kết pi và 2 nguyên tử oxi.
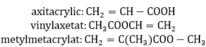
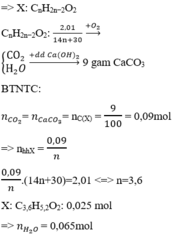


Đáp án A
nCO2 = 0,09 mol
Vì các chất đều gồm 2O và có 2π trong phân tử nên đặt CTC của hh là CnH2n - 2O2
CnH2n - 2O2 + O2 → nCO2 + (n - 1)H2O
(14n+30)gam---------------n mol
2,01 gam------------------0,09 mol
→ 2,01n = 0,09(14n + 30) → n = 3,6 → nH2O = 0,09 x 2,6 : 3,6 = 0,065 mol.
mdd giảm = m↓ - mCO2 - mH2O = 9 - 0,09 x 44 - 0,065 x 18 = 3,87 gam

Đáp án: A
Cả 3 chất trên đều có π trong phân tử
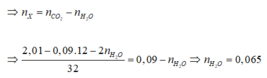
Khối lượng dung dịch X thay đổi:
∆
m
=
m
C
O
2
+
m
H
2
o
-
m
C
a
C
O
3
=
-
3
,
87
Vậy, khối lượng giảm 3,87 gam

Đáp án A
Cả 3 chất trên đều có 2π trong phân tử
⇒
n
X
=
n
C
O
2
-
n
H
2
O
⇒
2
,
01
-
0
,
09
.
12
-
2
n
H
2
O
32
⇒
n
H
2
O
=
0
,
065
Khối lượng dung dịch X thay đổi:
![]()
⇒ ∆ m = - 3 , 87
Vậy, khối lượng giảm 3,87 gam
Đáp án B
Hướng dẫn
Cả 2 chất trên đều có công thức phân tử là C2H6O.
Khi đốt cháy C2H6O → 2CO2
=> số mol CO2 = 0,8.2 = 1,6 mol.
=> Khối lượng kết tủa = 1,6.100 = 160 (gam)