Điện phân 500ml dung dịch chứa hỗn hợp gồm CuSO4 aM và NaCl 0,75M với điện cực tro cường độ dòng điện 5A . Sau thời gian điện phân 96,5 phút, khối lượng dung dịch giảm 17,15 gam. Giá trị của a là
A. 0,2
B. 0,5
C. 0,1
D. 0,4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

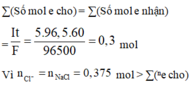
khối lượng dung dịch giảm chính là khối lượng của CuCl2 = x mol và HCl = y mol
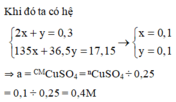
Đáp án A

Chọn đáp án A
∑(Số mol e cho) = ∑(Số mol e nhận) = I t F = 5 . 96 , 5 . 60 96500 = 0 , 3 mol
Vì n C l - = n N a C l = 0 , 375 mol > ∑(ne cho) ⇒ khối lượng dung dịch giảm chính là khối lượng của CuCl2 = x mol và HCl = y mol
Khi đó ta có hệ
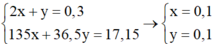
⇒ a = CMCuSO4 = nCuSO4 ÷ 0,25 = 0,1 ÷ 0,25 = 0,4M ⇒ Chọn A

Đáp án B
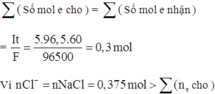
=>Khối lượng dung dịch giảm chính là khối lượng của CuCl2 = x mol và HCl = y mol
Khi đó ta có hệ
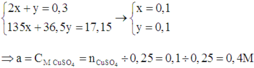

Đáp án B
ne = It/F = 5.(96,5.60)/96500 = 0,3 mol
nCl- (0,5) > ne (0,3) => Cl- chưa bị điện phân ở anot.
Giả sử Cu2+ chưa bị điện phân hết => nCu = 0,3/2 = 0,15 mol
nCl2 = 0,3/2 = 0,15 mol
m dung dịch giảm = mCu+mCl2 = 0,15.64 + 0,15.71 = 20,15 gam => Loại
=> Cu2+ bị điện phân hết, H2O đã bị điện phân ở catot.
Catot:
Cu2+ + 2e → Cu
x → 2x →x
H2O + 1e → OH- + 0,5H2
0,3-2x → 0,15-x
Anot:
Cl- - 1e → 0,5Cl2
0,3→ 0,15
m dung dịch giảm = mCu + mH2 + mCl2 => 17,15 = 64x + 2(0,15-x) + 0,15.71 => x = 0,1mol
=> a = 0,1/0,5 = 0,2 mol/lít
Giải thích: Đáp án A
ne = It/ F = 5. 96,5.60/96500 = 0,3 (mol)
Tại catot (-) Tại anot (+)
Cu2+ + 2e → Cu 2Cl- → Cl2 + 2e
0,5 a→ a → 0,5a 0,15 ← 0,3
2H2O + 2e → H2 + 2OH-
b → 0,5b
Nồng độ của CuSO4 = a = 0,2 M