Cho 1,37 gam kim loại kiềm thổ M phản ứng với nước (dư), thu được 0,01 mol khí H 2 . Kim loại M là
A. Ba
B. Sr
C. Mg
D. Ca
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
M + 2H2O → M(OH)2 + H2
Mol 0,01 ← 0,01
=> MM = 1,37: 0,01 = 137 g/mol (Ba)

Gọi kim loại cần tìm là R
$R + 2H_2O \to R(OH)_2 + H_2$
Theo PTHH :
$n_R = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$M_R = \dfrac{6}{0,15} = 40(đvC)$
Vậy R là Canxi. Chọn đáp án A
PTHH: 2M + 2xH2O ---> 2M(OH)x + xH2
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{x}.n_{H_2}=\dfrac{2}{x}.0,15=\dfrac{0,3}{x}\left(mol\right)\)
=> \(M_M=\dfrac{6}{\dfrac{0,3}{x}}=\dfrac{6x}{0,3}=20x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 |
| M | 20 | 40 | 60 |
| loại | Ca | loại |
Vậy M là canxi (Ca)
Chọn A

Đáp án B.
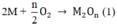
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
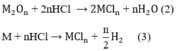
Số mol H2: 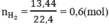
Theo phương trình (1)
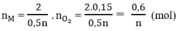
Theo phương trình (3)
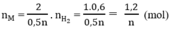
Tổng số mol M là 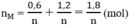
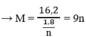
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Đáp án cần chọn là: A