Tập hợp ba thông số xác định trạng thái của một lượng khí xác định là
A. áp suất, thể tích, khối lượng.
B. áp suất, nhiệt độ, thể tích
C. nhiệt độ, áp suất, khối lượng.
D. thể tích, nhiệt độ, khối lượng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
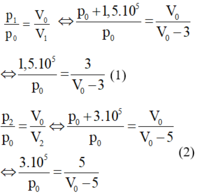
Từ (1) và (2), ta tìm được p 0 = 6 . 10 5 Pa; V 0 = 15 lít.

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
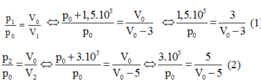
Từ (1) và (2), ta tìm được p0 = 6.105 Pa; V0 = 15 lít.

Chọn B.
Vì quá trình biến đổi là đẳng nhiệt nên ta có:
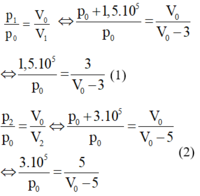
Từ (1) và (2), ta tìm được p0 = 6 . 10 5 Pa; V0 = 15 lít

Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m / V 0
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 . V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 . V 0 = pV (2)
Từ (1) và (2) suy ra:
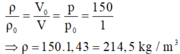
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g

Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m/ V 0 .
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 V 0 = pV (2)
Từ (1) và (2) suy ra:
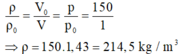
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g

Chọn A.
Ở điều kiện tiêu chuẩn (1 atm, 0 oC), khối lượng riêng của ôxi là: ρ0 = m/V0.
Ở điều kiện 150 atm, 0 oC, khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = ρ0.V0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p0V0 = pV (2)
Từ (1) và (2) suy ra:
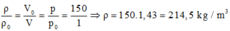
Và m = ρ.V = 214,5.15-3 ≈ 3,23 kg.

Chọn D.
Áp dụng định luật Bôi-lơ – Ma-ri-ốt, ta có p1V1 = p2V2
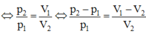
Suy ra p1 = 40 Pa.
Chọn B.
Tập hợp ba thông số trạng thái của khí lý tưởng bao gồm nhiệt độ (T), thể tích (V) và áp suất (p).