Một khối khí lí tưởng thực hiện quá trình đẳng áp ở hai áp suất khác nhau được biểu diễn như hình sau:

Quan hệ giữa p 1 v à p 2 là:
A. Không so sánh được
B. p 1 < p 2
C. p 1 = p 2
D. p 1 > p 2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án: B
Vận dụng kiến thức về đường đẳng tích. Dựa vào đò thị ta có thể suy ra V 1 > V 2

Đáp án: A
Ta có:
Lượng không khí trong bình được đun nóng trong một quá trình đẳng tích.
Trạng thái 1: t 1 = 120 K p 1 = ? a t m
Trạng thái 2: t 2 = 300 K p 2 = 4 a t m
Trong quá trình đẳng tích:
p 1 T 1 = p 2 T 2 ⇒ p 1 = p 2 . T 1 T 2 = 4. ( 120 + 273 ) ( 300 + 273 ) = 2,74 a t m

Đáp án: D
Ta có:
Lượng không khí trong bình được đun nóng trong một quá trình đẳng tích.
Trạng thái 1: t 1 = 400 K p 1 = 2,4 a t m
Trạng thái 2: t 2 = 800 K p 2 = ?
Trong quá trình đẳng tích:
p 2 T 2 = p 1 T 1 → p 2 = p 1 . T 2 T 1 = 2,4. ( 800 + 273 ) ( 400 + 273 ) ≈ 3,8 ( a t m )

Đáp án: B
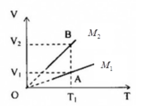
Vẽ đường thẳng qua T 1 , song song với trục OV, cắt đồ thị (V,T) của hai khí tại A p 1 , V 1 , T 2 và B p 1 , V 2 , T 1
Viết phương trình Cla-pe-rôn - Men-đê-lê-ép cho hai trạng thái, ta được:
p 1 V 1 = m M 1 R T 1 ( 1 ) p 1 V 2 = m M 2 R T 1 ( 2 )
Từ (1) và (2) suy ra: V 1 V 2 = M 2 M 1
Mặt khác, từ đồ thị, ta thấy: V 1 < V 2 ta suy ra M 2 < M 1

Đáp án: B
Đồ thị ở phương án B không biểu diễn đúng quá trình trên vì quá trình ở đầu bài là quá trình đẳng áp mà đồ thị B cho thấy áp suất thay đổi

Tóm tắt đề bài như sau:
\(\left\{{}\begin{matrix}V=10\left(l\right)\\p=2\left(atm\right)\\T=87+273=360\left(K\right)\end{matrix}\right.\underrightarrow{Đẳngáp}\left\{{}\begin{matrix}V_1=?\\p_1=2\left(atm\right)\\T_1=\dfrac{T}{2}=180\left(K\right)\end{matrix}\right.\) \(\underrightarrow{Đẳngnhiet}\left\{{}\begin{matrix}V_2=?\\p_2=0,5\left(atm\right)\\T_2=180\left(K\right)\end{matrix}\right.\)
Phương trình trạng thái khí lí tưởng ( Claperon Mendeleep ): \(\dfrac{pV}{T}=const\)
Đẳng áp: \(\dfrac{V}{T}=\dfrac{V_1}{T_1}\Leftrightarrow V_1=\dfrac{10.180}{360}=5\left(l\right)\)
Đẳng nhiệt: \(p_1V_1=p_2V_2\Rightarrow V_2=\dfrac{p_1V_1}{p_2}=\dfrac{2.5}{0,5}=20\left(l\right)\)
Vậy thể tích sau cùng của khối khí trên là V2=20(l)

\(T_1=27^oC=300K\)
Quá trình khí lí tưởng:
\(\dfrac{p_1V_1}{T_1}=\dfrac{p_2V_2}{T_2}\)
\(\Rightarrow\dfrac{1\cdot10}{300}=\dfrac{15\cdot2\cdot1}{T_2}\)
\(\Rightarrow T_2=900K=627^oC\)
Cho em hỏi ạ ⇒1.10/300=15.2.1 /T ngay chỗ 15.2.1 số 1 ơn đâu mà nhân vào ạ
Đáp án: B
Từ đồ thị, ta suy ra: p 1 < p 2