Cho 200ml dung dịch CuCl2 0,1 M tác dụng với dung dịch NaOH dư, thu được số gam kết tủa là
A. 1,96g B. 2,92g C. 0,98g D. 23,4g
Các bạn giúp mình với ! Mình cảm ơn rất nhiều
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$Ag^+ + Cl^- \to AgCl$
n Cl- = n AgCl = 86,1/143,5 = 0,6(mol)
Bảo toàn điện tích :
n Cu2+ = (0,6 + 0,2 - 0,1.3 + 0,2.2 )/2 = 0,05(mol)
Bảo toàn nguyên tố Fe,Cu,Mg , Kết tủa gồm :
Fe(OH)3 : 0,1 mol
Mg(OH)2 : 0,2(mol)
Cu(OH)2: 0,05(mol)
=> m kết tủa = 0,1.107 + 0,2.58 + 0,05.98 = 27,2 gam
Đáp án A

n Ba(OH)2 = 2.0,2=0,4 mol
\(Ba\left(OH\right)_2+SO_2->BaSO_3+H_2O\)
0,4 ................0,4...........0,4
m BaSO3 = 0,4. ( 138+32+16.3)=87,2 g
v SO2 = 0,4.22,4=8,96 lít
m BaSO3 = 0,4. ( 137+32+16.3)=86,8 g
xin lũi nha mình nhìn nhầm bạn thông cảm

a.CuCl2 + 2NaOH -> Cu(OH)2 + 2NaCl
0.15 0.3 0.15 0.3
Cu(OH)2 -> CuO + H2O
0.15 0.15
nNaOH = 0.3 mol
\(CM_{CuCl2}=\dfrac{0.15}{2}=0.075M\)
b.Vdd sau phản ứng = 0.2 + 0.15 = 0.35l
\(CM_{NaCl}=\dfrac{0.3}{0.35}=0.86M\)
c.mCuO = \(0.15\times80=12g\)

Al + 4HNO3 --> Al(NO3)3 + NO + 2H2O
Fe + 4HNO3 --> Fe(NO3)3 + NO + 2H2O
Dung dịch B gồm có Al(NO3)3, Fe(NO3)3 và HNO3. Chất kết tủa là Al(OH)3 và Fe(OH)3.
Đặt a, b là số mol của Al và Fe. Thiết lập hệ phương trình để tìm a và b.
nNO = a + b = 0.5 mol.
m kết tủa = 78a + 104 b = 41.9 gam
giải ra a = 0.4 , b = 0.1.
Suy ra khối lượng hỗn hợp kim loại m = 27*0.4 + 56*0.1 =16.4 gam
Tính %mAl = (0.4*27*100)/16.4 = 65.85%, %mFe = 43.15%
Chúc bạn học tốt nhé. Không hiểu thì inbox mình nhé :D
Chào bạn

\(n_{AgNO_3}=0,2.2=0,4\left(mol\right)\)
\(AgNO_3+KCl\rightarrow AgCl+KNO_3\)
0,4 0,4
\(m_{kt}=0,4.143,5=57,4\left(g\right)\)

Đáp án B
Gọi số mol các ion K+, HCO3-, Cl- và Ba2+ có trong 100 ml dung dịch lần lượt là x, y, z, t mol
-Phần 1: HCO3-+ OH-→ CO32-+ H2O
y y y
Ba2++ CO32-→ BaCO3
t y t mol = 0,1 mol
-Phần 2:
HCO3-+ OH-→ CO32-+ H2O
y y y
Ba2++ CO32-→ BaCO3
y y = 0,15
-Phần 3:
Ag++ Cl-→ AgCl
2z 2z = 0,2 mol suy ra z = 0,1 mol
Theo ĐLBT ĐT thì: x+2t=y+z suy ra x=0,05 mol
đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
(39x+ 61y + 35,5.z+ 137t)/2= 14,175 gam

Nhận thấy lượng kết tủa thu được khi cho vào NaOH nhỏ hơn khi cho X vào Ba(OH)2
→ n(Ba2+) < n(HCO3-)
Trong phần 1 → n(Ba2+) = 9,85 : 197 = 0,05 mol
Trong phần 2 → n(HCO3-) = 15,76 : 197 = 0.08 mol
Bảo toàn điện tích → n(Na+) = 0,08 + 0,12 – 0,05.2 = 0,1 mol
Khi đun sôi thu được muối chứa Na+ : 0,1 mol, Ba2+ : 0,08 mol, Cl- : 0,12 mol, CO3- : 0,04 mol
→ m = 2.(0,1.23 + 0,05.137 + 0,12.35,5 + 0,04.60) = 31,62 gam
→ Đáp án C

Đáp án C.
1/2 X tác dụng với dung dịch NaOH thu được ít kết tủa hơn khi tác dụng với dung dịch Ba(OH)2, nên khi tác dụng với NaOH thì Ba2+ hết.
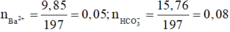
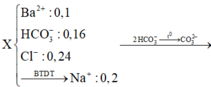
![]()
![]()
A
chọn đáp án A