1) cho 50ml dung dịch A gồm Na2CO3 1M và (NH4)2CO3 1,5M tác dụng vừa đủ với Ca(NO3)2 2M và Ba(OH)2 0,5M thu được m gam kết tủa và dung dịch C.
a) tính m
b) tính nồng độ các ion trong dung dịch C
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{Ca\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
PT: \(Ca\left(OH\right)_2+Na_2CO_3\rightarrow CaCO_{3\downarrow}+2NaOH\)
_______0,2_______0,2________0,2 (mol)
\(\Rightarrow C_{M_{Na_2CO_3}}=\dfrac{0,2}{0,25}=0,8\left(M\right)\)
\(m_{CaCO_3}=0,2.100=20\left(g\right)\)

a.
\(Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+2NaOH\)
b.
\(n_{BaCO_3}=n_{Na_2CO_3}=0,2.1=0,2\left(mol\right)\\ m_{kt}=197.0,2=39,4\left(g\right)\)
c.
\(n_{Ba\left(OH\right)_2}=n_{Na_2CO_3}=0,2\left(mol\right)\\ C\%_{Ba\left(OH\right)_2}=\dfrac{0,2.171.100\%}{200}=17,1\%\)

\(n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ n_{H_3PO_4}=0,3\left(mol\right)\\ Vì:\dfrac{n_{Ca\left(OH\right)_2}}{n_{H_3PO_4}}=\dfrac{0,3}{0,3}=1\\ \Rightarrow Tạo.1.muối:CaHPO_4\\ Ca\left(OH\right)_2+H_3PO_4\rightarrow CaHPO_4+2H_2O\\ m_{\downarrow}=0\\ n_{CaHPO_4}=n_{Ca\left(OH\right)_2}=0,3\left(mol\right)\\ C_{MddCaHPO_4}=\dfrac{0,3}{0,3+0,3}=0,5\left(M\right)\)

a, \(n_{Ba\left(OH\right)_2}=0,1.0,1=0,01\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,02\left(mol\right)\)
\(n_{NaOH}=0,1.0,1=0,01\left(mol\right)=n_{Na^+}=n_{OH^-}\)
⇒ ΣnOH- = 0,02 + 0,01 = 0,03 (mol)
\(n_{H_2SO_4}=0,4.0,0175=0,007\left(mol\right)=n_{SO_4^{2-}}\)
\(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,014\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,014___0,014 (mol) ⇒ nOH- dư = 0,03 - 0,014 = 0,016 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,007____0,007_____0,007 (mol) ⇒ nBa2+ dư = 0,01 - 0,007 = 0,003 (mol)
⇒ m = 0,007.233 = 1,631 (g)
\(\left[OH^-\right]=\dfrac{0,016}{0,1+0,4}=0,032\left(M\right)\)
\(\left[Ba^{2+}\right]=\dfrac{0,003}{0,1+0,4}=0,006\left(M\right)\)
\(\left[Na^+\right]=\dfrac{0,01}{0,1+0,4}=0,02\left(M\right)\)
b, pH = 14 - (-log[OH-]) ≃ 12,505
\(n_{Ba^{2+}}=0,1.0,1=0,01\left(mol\right)\)
\(n_{SO_4^{2-}}=0,4.0,0175=7.10 ^{-3}\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\downarrow\)
\(\Rightarrow m=m_{BaSO_4}=7.10^{-3}.233=1,631\left(g\right)\)
Ta có:
\(n_{H^+}=0,4.0,0175.2=0,014\left(mol\right)\)
\(n_{OH^-}=0,1.0,1.2+0,1.0,1=0,03\left(mol\right)\)
Trong dung dịch X:
\(n_{OH^-}=0,03-0,014=0,016\left(mol\right)\)\(\Rightarrow\left[OH^-\right]=\dfrac{0,016}{0,1+0,4}=0,032\left(M\right)\)
\(n_{Ba^{2+}}=0,01-7.10^{-3}=3.10^{-3}\left(mol\right)\Rightarrow\left[Ba^{2+}\right]=\dfrac{3.10^{-3}}{0,1+0,4}=6.10^{-3}\left(M\right)\)
\(n_{Na^+}=0,1.0,1=0,01\left(mol\right)\Rightarrow\left[Na^+\right]=0,02\)
\(pOH=-lg\left(0,032\right)\approx1,5\Rightarrow pH=14-1,5=12,5\)

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+Fe\left(OH\right)_2\downarrow\)
Ta có: \(n_{H_2SO_4}=0,3\cdot0,5=0,15\left(mol\right)=n_{Fe}=n_{H_2}=n_{Ba\left(OH\right)_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,15\cdot56=8,4\left(g\right)\\V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\V_{Ba\left(OH\right)_2}=\dfrac{0,15}{1}=0,15\left(l\right)=150\left(ml\right)\end{matrix}\right.\)
*Bạn xem lại đề vì nếu FeSO4 p/ứ hết thì sẽ có nhiều hơn 41,7 gam kết tủa

Đáp án A
Có n H C l = 0 , 15 ; n C O 2 = 0 , 045 ; n B a C O 3 = 0 , 15
Gọi n N a 2 C O 3 = a ; n N a H C O 3 = b
Các phản ứng xảy ra theo thứ tự sau:
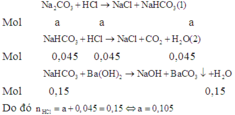
Áp dụng định luật bảo toàn nguyên tố C, ta có:
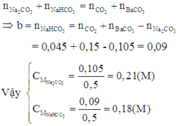

Đáp án B
Ta có: nHCl = 0,15 mol; n C O 2 = 1,008/22,4 = 0,045 mol.
Giả sử ban đầu có x mol NaHCO3
CO32- + H+ → HCO3- (1)
HCO3-+ H+ → CO2+ H2O (2)
0,045 0,045 ←0,045
Theo PT (2): n H C O 3 - = n H + = n C O 2 = 0,045 mol
→ n H + PT1 = 0,15- 0,045= 0,105 mol
→ n C O 3 2 - PT1 = n H + = n H C O 3 - PT1 = 0,105 mol
→ n N a 2 C O 3 = n C O 3 2 - PT1= 0,105 mol
→ C M N a 2 C O 3 = 0,105/ 0,5 = 0,21M
Dung dịch Y chứa Na+, HCO3- dư:
x+0,105- 0,045 = x+0,06 mol
HCO3-+ OH- → CO32-+ H2O
Ba2++ CO32- → BaCO3
Ta thấy: n H C O 3 - = n C O 3 2 - = n B a C O 3 = 29,55/197 = 0,15 mol
→ x+0,06 = 0,15
→ x = 0,09 mol → C M N a H C O 3 = 0,09/ 0,5 = 0,18M

\(n_{HCl}=Cm.V=1.0,1=1mol\)
\(n_{H_2SO_4}=Cm.V=0,5.0,1=0,05mol\)
Thể thích của dd D là 200ml = 0,2l
\([H^+]=\frac{n_{HCl}+2.n_{H_2SO_4}}{V}=\frac{0,1+0,1}{0,2}=1M\)
\([Cl^-]=\frac{n_{HCl}}{V}=\frac{0,1}{0,2}=0,5M\)
\([SO_4^{2-}]=\frac{n_{H_2SO_4}}{V}=\frac{0,05}{0,2}=0,25M\)
Khi cho dd D vào \(Ba\left(OH\right)_2\) chỉ có \(H_2SO_4\) tác dụng, tạo kết tủa
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
\(0,05....\rightarrow0,05mol\)
\(\rightarrow m_{BaSO_4}=n.M=0,05.233=11,65g\)