Hòa tan hh X gồm Fe và Mg bằng 1 lượng vừa đủ HCL 20% thu được dd Y. Biết nồng độ của MgCl2 trong dd Y là 11.787%
A. Tính nồng độ của muối sắt
B. Nếu thêm vào dd Y 1 lượng dd NaOH 10% vừa đủ để tác dụng thì nồng độ % của các chất có trong dd sau phản ứng là bao nhiêu.

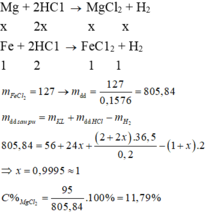




Giả sử \(m_{ddHCl}=36,5(g) ->n_{HCl}=\dfrac{36,5.20}{36,5.100}=0,2(mol) \)
Gọi a và b là số mol của Fe và Mg
\(Fe+2HCl\)→\({FeCl_2}+H_2\)
\(Mg+2HCl\)→\({MgCl_2}+H_2\)
→\(2a+2b=0,2\)
→\(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,1 mol\)
Vậy khối lượng dung dịch sau phản ứng:
→\(m_Y=m_{Fe}+m_{Mg}+m_{ddHCl}-m_{H_2}\)
→\(m_Y=(56a+24b+36,3)g \)
→C%\({MgCl_2}=\dfrac{95b}{56a+24b+36,3}.100=11,787\)
→\(660,72-9217,112b=-427,8681\)
→\(\begin{cases} 2a+2b=0,2\\ 660,072a-9217,112b=-427,8681 \end{cases}\)
→\(a=b=0,05\)
→C%\({FeCl_2}=\dfrac{127.0,05}{56.0,05+24.0,05+36,3}.100=15,76%\)%
b)Giả sử \(m_{NaOH}=40g \)
\(2NaOH+{FeCl_2}\)→\(2NaCl+{Fe(OH)_2}\)
\(2NaOH+{MgCl_2}\)→\(2NaCl+{Mg(OH)_2}\)
Vì phản ứng vừa đủ nên dung dịch sau phản ứng chỉ có NaCl
→\(m_{ddNaOH}=\dfrac{40.100}{10}=400g\)
→\(m_{dd}=m_{ddNaOH}+m_{FeCl_2}+m_{MgCl_2}-m_{Fe(OH)_2}-m_{Mg(OH)_2}\)
→\(m_{dd}=403,7(g) \)
→\(n_{NaCl}=2(n_{FeCl_2}+n_{MgCl_2})=0,2mol\)
→C%\(NaCl=\dfrac{0,2.58,5}{403,7}.100=2,89\)%
Hóa học là môn mình học dốt nhất