Bằng cách nào sau đây có thể pha chế được dd Nacl 15%
A Hòa tan 25 g NaCl vào 90d H2O
B Hòa tan 15 g NaCl vào 100g H2O
C Hòa tan 30 g NaCl vào 170g H2O
D Hòa tan 15g NaCl vào 185g H2O
GIÚP MÌNH CÁCH TÍNH RA VỚI!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{NaCl}=15\left(g\right)\Rightarrow m_{ddNaCl}=\dfrac{100.15}{15}=100\left(g\right)\\ \Rightarrow m_{H_2O}=100-15=85\left(g\right)\Rightarrow Loại:A,B,D\\ m_{NaCl}=30\left(g\right)\Rightarrow m_{ddNaCl}=\dfrac{30.100}{15}=200\left(g\right)\\ \Rightarrow m_{H_2O}=200-30=170\left(g\right)\Rightarrow C.đúng\\ Chọn.C\)

Không có đáp án đúng
m NaCl = 15 gam
=> m dd = 15/15% = 100(gam)
=> m H2O = 100 -15 = 85 gam

\(a,m_{NaCl}=\dfrac{8.200}{100}=16\left(g\right)\\ b,m_{HCl}=\dfrac{250.14}{100}=35\left(g\right)\\ m_{H_2SO_4}=\dfrac{19,6.300}{100}=58,8\left(g\right)\)

a) \(m_{NaCl}=\dfrac{8.200}{100}=16\left(g\right)\)
b) \(m_{HCl}=\dfrac{14.250}{100}=35\left(g\right)\)
c) \(m_{H_2SO_4}=\dfrac{19,6.300}{100}=58,8\left(g\right)\)

\(a,C\%_{NaCl}=\dfrac{15}{15+185}.100\%=7,5\%\\ b,m_{HNO_3}=\dfrac{18,9}{100}.100+\dfrac{6,3}{100}.200=31,5\left(g\right)\\ m_{ddHNO_3}=100+200=300\left(g\right)\\ C\%_{HNO_3}=\dfrac{31,5}{300}.100\%=10,5\%\)
\(c,n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\\ C_{M\left(NaCl\right)}=\dfrac{0,1}{0,1}=1M\\ d,n_{KOH}=2.0,2+0,2.0,2=0,44\left(mol\right)\\ V_{ddKOH}=0,2+0,2=0,4\left(l\right)\\ C_{M\left(KOH\right)}=\dfrac{0,44}{0,4}=1,1M\\ e,m_{NaOH}=\dfrac{150.16}{100}=24\left(g\right)\\ m_{ddNaOH}=50+150=200\left(g\right)\\ C\%_{NaOH}=\dfrac{24}{200}.100\%=12\%\)

Ở 20 0 C thì 75g nước hòa tan tối đa muối NaCl có khối lượng:
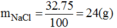
Vậy dung dịch NaCl đã pha chế là chưa bão hòa. Để dung dịch NaCl bão hòa ở nhiệt độ này, ta cần cho thêm vào dung dịch đã pha chế một lượng NaCl là: 24-23,5=0,5(g)

a) Ta có: \(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,1}{0,5}=0,2\left(M\right)=\left[Na^+\right]=\left[Cl^-\right]\)
b) Ta có: \(n_{Ba\left(OH\right)_2}=\dfrac{34,2}{171}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[Ba^{2+}\right]=0,4\left(M\right)\\\left[OH^-\right]=0,8\left(M\right)\end{matrix}\right.\)
c) Ta có: \(n_{H_2SO_4}=0,025\cdot2=0,05\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,05}{0,125+0,025}\approx0,33\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[H^+\right]=0,66\left(M\right)\\\left[SO_4^{2-}\right]=0,33\left(M\right)\end{matrix}\right.\)