Bài 1: Viết PTHH phản ứng cháy của các chất sau trong oxi: H2; Mg; Cu; S; Al; C và P.
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a) khi có 6,4g khí oxi tham gia phản ứng
b) khi đốt 6gam cacbon trong bình đựng 19,2 gam khí oxi
Bài 3: Khi đốt khí metan (CH4); khí axetilen (C2H2), rượu etylic (C2H6O) đều cho sản phẩm là khí cacbonic và hơi nước. Hãy viết PTHH phản ứng cháy của các phản ứng trên
Bài 4: Tính lượng oxi cần dùng để đốt cháy hết:
a) 46,5 gam Photpho b) 67,5 gam nhôm c) 33,6 lít hiđro
Bài 5: Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy.
b) Tính số gam oxi còn dư sau phản ứng cháy.
Bài 6: Hãy cho biết 3. 1024 phân tử oxi có thể tích là bao nhiêu lít?
Bài 7: Đốt cháy 6,2 gam photpho trong bình chứa 6,72 lít khí oxi (đktc) tạo thành điphotpho pentaoxit.
a) Chất nào còn dư sau phản ứng, với khối lượng là bao nhiêu?
b) Tính khối lượng sản phẩm tạo thành.
Bài 8: Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và thể tích oxi cần dùng để có thể điều chế được 2,32 gam oxit sắt từ
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên.
Bài 9: Đốt 5,6gam hỗn hợp cacbon và lưu huỳnh cần 9,6 gam khí oxi
a) Viết PTHH các phản ứng xảy ra
b) Tính khối lượng của mỗi chất trong hỗn hợp ban đầu
c) Tính thành phần phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu
d) Tính thành phần phần trăm theo số mol của mỗi chất có trong hỗn hợp khí thu được sau phản ứng
Bài 10: Có 2 lọ thuỷ tinh, một lọ đựng khí oxi, một lọ đựng không khí. Hãy nêu cách phân biệt 2 lọ.
Bài 11: Tính khối lượng oxi cần dùng để đốt cháy hoàn toàn 1 tấn than chứa 95% cacbon. Các tạp chất còn lại không cháy.
Bài 12: Viết những PTHH biểu diễn sự oxi hóa:
a) Đơn chất: Al, Zn, Fe, Cu, Na, C, S, P.
b) Hợp chất: CO, CH4, C2H2, C2H6O

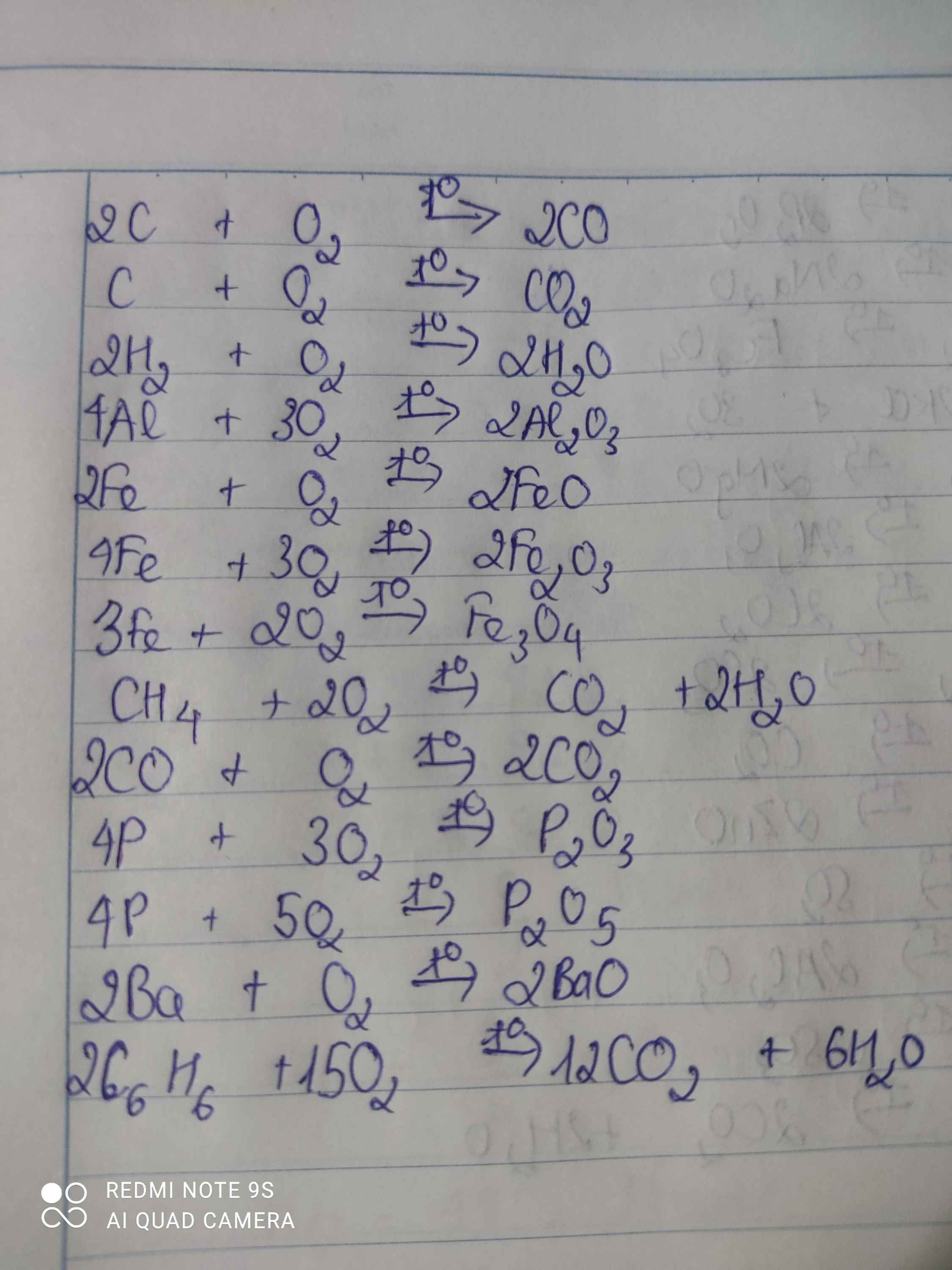
1.
H2+ 1/2O2 --to> H2O
Mg + 1/2O2 --to> MgO
Cu+ 1/2O2--to>CuO
S+O2 --to>SO2
4Al+ 3O2--to>2Al2O3
C+ O2--to> CO2
2P+5/2O2--to> P2O5
b2
a)
C+O2to→CO2
nCO2=6,4\32=0,2
=>nCO2=nO2=0,2 mol
mCO2=0,2x44=8,8 g
b)
nC=6\12=0,5
nO2=19,2\32=0,6
C+O2to→CO2
TPU 0,5 0,6
PU 0,5 0,5 0,5
SPU 0 0,1 0,5
mCO2=0,5x44=22 g
b3
CH4+2O2to→CO2+2H2O
2C2H2+5O2to→4CO2+2H2O
C2H6O+3O2to→2CO2+3H2O
b4
a)
4P+5O2->2P2O5
nP=46,5/31=1,5 mol
=>nO2=1,5x5/4=1,875 mol
mO2=1,875x32=60 g
b)
nC=30/12=2,5 mol
C+O2->CO2
2,5 2,5
mO2=2,5x32=80 g
c)
nAl=67,5/27=2,5 mol
4Al+3O2->2Al2O3
2,5 1,875
mO2=1,875x32=60 g
d)
nH2=33,6/22,4=1,5 mol
2H2+O2->2H2O
1,5 0,75
mO2=32x0,75=24 g
b5
a,
nO2= 0,46875 mol
nSO2= 0,3 mol
S+ O2 -> SO2
=> O2 dư 0,16875 mol. Có 0,3 mol S cháy
mS= 9,6g
b,
mO2 dư= 5,4g
b6
CÓ nO2 = S/6.1023 = 3.1024 / 6. 1023 = 5 (mol)
=> VO2 = n x 22.4 = 5 x 22.4 =112(l)
b7
4P+5O2=to=>2P2O5
nP=6,2\31=0,2(mol);nO2=6,72\22,4=0,3(mol)
Theo PTHH, ta có: 0,2\4<0,3\5=>O2 dư
nO2(dư)=0,3−(0,2.5\4)=0,05(mol)
mO2(dư)=0,05.32=1,6(g)
nP2O5=2\4.nP=2\4.0,2=0,1(mol)
mP2O5=0,1.142=14,2(g)
b8
a. Số mol oxit sắt từ : nFe3O4=2,32\(56.3+16.4) = 0,01 (mol).
Phương trình hóa học.
3Fe + 2O2 -to> Fe3O4
3mol 2mol 1mol.
.................................... 0,01 mol.
Khối lượng sắt cần dùng là : m = 56.3.0,011=1,6856.3.0,01\1=1,68 (g).
Khối lượng oxi cần dùng là : m = 32.2.0,011=0,6432.2.0,01\1=0,64 (g).
b. Phương trình hóa học :
2KMnO4 to-> K2MnO4 + O2
2mol 1mol
n = 0,04 0,02
Số gam penmangarat cần dùng là : m= 0,04. (39 + 55 +64) = 6,32 g.
b9b11
a) PTHH: C + O2 → CO2 ↑
Đổi: 1 tấn = 1000000 gam
Khối lượng của C trong than là: 1000000.95% = 950000 gam
Số mol của C là: 950000:12 = 79166,67 mol
Số mol của O2 = 79166,67 mol
Khối lượng ôxi cần dùng là: 79166,67 . 32 = 2533333,44 gam
Em thật sự sợ chị lắm rồi đấy.
Chụp ảnh rồi ngồi cắm mặt vào gõ phím, chị ko đau tay à?