Cho 15,92g hỗn hợp A gồm NaX, NaY(X,Y là hia halogen ở hai chu kì liên tiếp và Mx<My vào nước được dung dịch B. Cho dd B tác dụng với dd AgNO3 dư, thu được 28,67g kết tủa. Tìm công thức NaX,NaY biết mNaX>mNaY
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn A
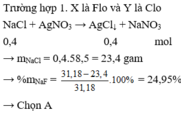
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
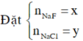
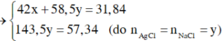
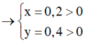
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
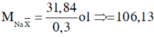
=> 2 muối là NaBr và NaI
Đáp án A

Quy NaX và NaY về NaR
\(n_{AgNO_3}=0,15.0,2=0,05\left(mol\right)\)
PTHH: \(AgNO_3+NaR\rightarrow AgR\downarrow+NaNO_3\)
0,05------>0,05
\(\rightarrow M_R=\dfrac{2,2}{0,05}=44\left(g\text{/}mol\right)\)
Mà X và Y là 2 nguyên tố halogen thuộc 2 chu kì liên tiếp
\(\rightarrow M_X< M_R< M_Y\rightarrow M_X< 44< M_Y\)
---> X và Y là Cl và Br

Cái chỗ M đó suy ra là \(M_X< 83,13< M_Y\)
Thì có 2 chất liên tiếp là Br (80) và I (127)

Gọi công thức chung là NaR
\(NaR+AgNO_3\rightarrow AgR+NaNO_3\)
\(n_{AgR}=\frac{28,67}{108+R}\)
\(n_{NaR}=\frac{15,92}{23+R}\)
Ta có :nAgR=nNaR
\(\Leftrightarrow\frac{15,92}{23+R}=\frac{28,67}{108+R}\)
\(\rightarrow R=83,13\)
\(\rightarrow Al\left(Br\right)< R< A_2\left(I_2\right)\)
\(\rightarrow NaBr,NaI\)



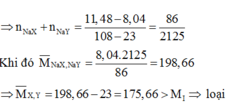
\(NaM+AgNO_3\rightarrow AgM+NaNO_3\)
\(n_{NaM}=n_{AgM}\)
\(\Leftrightarrow\frac{15,92}{23+M_M}=\frac{28,67}{108+M_M}\)
\(\Rightarrow M_M=83,333\)
\(\Rightarrow\) X là Brom(Br) ;Y là Iot(I)
Vậy NaX là NaBr và NaY là NaI