Khi cho 500ml dung dịch NaOH 1M tác dụng hết với dung dịch HCl 3,5M . Khối lượng mỗi oxit trong hỗn hợp là:
A. 4 g và 16 g | B. 10 g và 10 g | C. 8 g và 12 g | D. 14 g và 6 g. |
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
NaOH + HCl → NaCl + H2O
x(mol) x(mol)
KOH + HCl → KCl + H2O
y(mol) y(mol)
gọi x, y lần lượt là số mol NaOH và KOH
theo bài ra ta có hệ pt
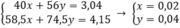
mNaOH = 0,02.40 = 0,8 (g)
mKOH = 0,04.56 = 2,24 (g)

Tương tự công thức câu 18 ta thu được:
nhh = 0,25 (mol)
Gọi x và y lần lượt là số mol của H2NCH2COOH va CH3CH(NH2)COOH. Ta có hệ sau:
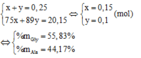

a/ Tính C% của dd KOH nhé, bạn viết sai đề![]()
mHCl = 20 x 18,25% = 3,65 gam
=> nHCl = 3,65 / 36,5 = 0,1 mol
PTHH: HCl + KOH ===> KCl + H2O
0,1 0,1 [ mol ]
Lập các số mol theo PT, ta có:
mKOH = 0,1 x 56 = 5,6 gam
=>C%KOH = 5,6 / 50 x 100% = 11,2%
2/ Gọi số mol của Fe2O3 và MgO lần lượt là x(mol), y (mol), ta có
PTHH: Fe2O3 + 3HCl ===>2 FeCl3 + 3H2O
x 3x (mol)
MgO + 2HCl ===> MgCl2 + H2O
y 2y (mol)
nHCl = 0,25 x 2 = 0,7 mol = x + y
Ta có hệ phương trình:
\(\begin{cases}3x+2y=0,7\\160x+40y=18\end{cases}\)
Giải hệ phương trình, ta đc x = 0,04 mol
y = 0,29 mol
=> mFe2O3 = 0,04 x 160 = 6,4 gam
mMgO = 0,29 x 40 = 11,6 gam

\(n_{Al_2O_3}=a\left(mol\right)\)
\(n_{MgO}=b\left(mol\right)\)
\(m_A=102a+40b=16.2\left(g\right)\left(1\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(m_{Muối}=267a+111b=40.95\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.249,b=-0.23\)
Sai đề !
Hỗn hợp nào vậy bn
đề bài không có bạn ạ