Bài 1: Lập công thức bazơ ứng với các oxit sau đây: CuO, FeO, BaO, MgO.
Bài 2: Kẽm tác dụng với axit sunfuric theo sơ đồ sau:
Zn + H2SO4 ---> ZnSO4 + H2
Có 13g kẽm tham gia phản ứng. Tính:
a) Khối lượng axit tham gia phản ứng.
b) Khối lượng muối ZnSO4 tạo thành.
c) Thể tích khí hiđro thu được sau phản ứng (ở đktc)
Bài 3: Người ta nung canxi cacbonat (CaCO3) ở nhiệt độ cao, thu được canxi oxit (CaO) và 5,6 lít khí cacbonic (CO2).
a) Viết PTHH.
b) Tính khối lượng CaCO3 tham gia phản ứng.
c) Tính khối lượng CaO thu được sau phản ứng.

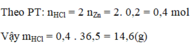
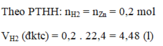

Bài1:
CuO: Cu(OH)2
FeO: Fe(OH)2
BaO: Ba(OH)2
MgO: Mg(OH)2
Bài 2
a) \(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 -->ZnSO4 + H2
0,2 ---> 0,2 --------> 0,2 --> 0,2 (mol)
=> \(m_{H2SO4}=0,2.98=19,6\left(g\right)\)
b) \(m_{ZnSo4}=0,2.161=32,2\left(g\right)\)
c) \(V_{H2}=0,2.22,4=4,48\left(l\right)\)
Bài 3:
\(n_{CO2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
a) PTHH: CaCO3 --to--> CaO + CO2
b) PTHH: CaCO3 --to--> CaO + CO2
0,25 <---------- 0,25 <-- 0,25 (mol)
=> \(m_{CaCO3}=0,25.100=25\left(g\right)\)
c) \(m_{CaO}=0,25.56=14\left(g\right)\)