Đốt cháy hoàn toàn 6,2 g P trong bình chứa 8,96 lít khí oxi (đktc) sản phẩm thu
được là chất rắn màu trắng. Nếu hiệu suất phản ứng là 80% thì khối lượng chất
rắn thu được là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

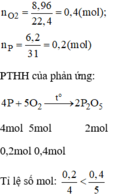
→ Oxi dư, vậy bài toán tính theo số mol của P
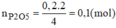
Do H = 80% nên khối lượng chất rắn thu được sau phản ứng là:
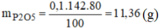

\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(n_{O_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(4P+5O_2\underrightarrow{^{^{t^0}}}2P_2O_5\)
\(4........5\)
\(0.2.........0.4\)
Lập tỉ lệ : \(\dfrac{0.2}{4}< \dfrac{0.4}{5}\Rightarrow O_2dư\)
\(n_{P_2O_5}=0.2\cdot\dfrac{2}{4}=0.1\left(mol\right)\)
\(m_{P_2O_5}=0.1\cdot142=14.2\left(g\right)\)
\(m_{P_2O_5\left(tt\right)}=14.2\cdot80\%=11.36\left(g\right)\)

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{4}< \dfrac{0,4}{5}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=0,25\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,15.32=4,8\left(g\right)\)
c, Theo PT: \(n_{P_2O_5}=\dfrac{1}{2}n_P=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(m_{P_2O_5}=14,2.80\%=11,36\left(g\right)\)

PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{3}< \dfrac{0,3}{2}\) , ta được O2 dư.
Mà: H% = 80% \(\Rightarrow n_{Fe\left(pư\right)}=0,3.80\%=0,24\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,3.0,24=0,06\left(mol\right)\)
Theo PT: \(n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,1\left(mol\right)\)
Chất rắn thu được gồm Fe dư và Fe3O4.
⇒ mcr = mFe (dư) + mFe3O4 = 0,06.56 + 0,1.232 = 26,56 (g)
Bạn tham khảo nhé!

\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,4}{5}\Rightarrow O_2dư\)
\(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=\dfrac{5}{4}.0,2=0,25\left(mol\right)\\ n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(n_{P_2O_5\left(lt\right)}=\dfrac{1}{2}n_P=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2\left(g\right)\\ m_{P_2O_5\left(tt\right)}=0,1.142.80\%=11,36\left(g\right)\)

TL:
a, PTHH:
4P + 5O2 -> 2P2O5
b,
Theo đề bài ta có:
nP= m/M=6,2 : 31 = 0,2 ( mol )
nO2 = V/22,4 = 8,96: 22,4 = 0,4 ( mol )
Theo PTPƯ ta có :
nP = 4/5nO2= 4/5 * 0,4 = 0,32 mol
-sản phẩm tạo thành là P2O5
Theo PTPƯ ta có :
nP2O5=2/5nO2=2/5 * 0,4 = 0,16 mol
->mP2O5 = n*M = 0,16 * 142 = 22,72 ( g )
Bài này O2 dư so với P, do đó sản phẩm P2O5 phải tính theo P.
nP2O5 = 1/2nP = 0,1 mol ---> mP2O5 = 0,1.142 = 14,2 g.

Bài 2:
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
PTHH: 4P + 5O2 → 2P2O5
Mol: 0,4 0,2
\(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
Bài 1:
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 4Al + 3O2 ---to→ 2Al2O3
Mol: 0,4 0,3
\(V_{O_2}=0,3.22,4=6,72\left(l\right)\)

a, 2Mg + O2 \(\underrightarrow{t^o}\) 2MgO
b, \(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(n_{O_2}=\dfrac{0,2}{2}=0,1mol\)
\(m_{O_2}=0,1.32=3,2g\)
\(V_{O_2}=0,1.22,4=2,24l\)
c, Cách 1:
\(Theo.ĐLBTKL,ta.có:\\ m_{Mg}+m_{O_2}=m_{MgO}\)
\(\Rightarrow m_{MgO}=4,8+3,2=8g\)
Cách 2:
\(n_{MgO}=\dfrac{0,2.2}{2}=0,2mol\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)
\(PTHH:4P+5O_2\rightarrow2P_2O_5\)
Ta có :
\(n_{O2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(\rightarrow m_{O2}=0,4.32=12,8\left(g\right)\)
Áp dụng ĐL bảo toàn KL:
\(m_P+m_{O2}=m_{P2O5}\)
\(m_{P2O5}=6,2+12,8=19\left(g\right)\)
Vì H = 80 %
\(\rightarrow m_{P2O5}=\frac{19.80}{100}=15,2\left(g\right)\)