1.Tính khối lượng mol của các chất sau:H2O,Al2O3,Mg3(PO4)2,Ca(OH)2
2.Tíh thành phần % (theo khối lượng)các nguyên tố hóa học có trong các hợp chất sau:MgO,Fe2O3
3.Tính khối lượng của 4,48 lít khí SO3(ở đktc)
Tính thể tích ở đktc của 6,4 gam khí CH4
4.Lập công thức hóa học và tính khối lượng mol của hợp chất gồm Al(III)liên kết với nhóm SO4(II)
(Cho biết H=1,O=16,Al=27,Ca=40,P=31,Mg=34,S=32,C=12,Fe=56)
5.Hợp chất A chứa nguyên tố Fe và O.Trong phân tử A có 7 nguyên tử và MA=232(g/mol).Tìm coogn thức hóa học của A
(Cho biết:S=32,O=16,Al=27,H=1,Fe=56,C=12)
giúp với ạ mình đang cần gấp

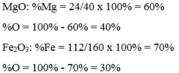

1.
\(M_{H2O}=2M_H+M_O=2.1+16=18\left(đvC\right)\)
\(M_{Al2O3}=2M_{Al}+3M_O=2.217+3.16=102\left(đvC\right)\)
\(M_{Mg3\left(PO4\right)2}=3m_{Mg}+2M_P+8M_O=2.34+2.31+8.16=262\left(đvC\right)\)
\(M_{Ca\left(OH\right)2}=M_{Ca}+2M_O+2M_H=1.40+2.16+2.1=74\left(đvC\right)\)
2.
Ta có: \(M_{MgO}=M_{Mg}+M_O=24+16=40\)
\(\rightarrow\%_{Mg}=\frac{24}{40}=60\%\rightarrow\%_O=40\%\)
\(M_{Fe2O3}=2M_{Fe}+3M_O=56.2+16.3=160\)
\(\rightarrow\%_{Fe}=\frac{56.2}{160}=70\%\rightarrow\%_O=30\%\)
3.
\(n_{SO3}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(m_{SO3}=0,2.80=16\left(g\right)\)
\(n_{CH4}=\frac{6,4}{16}=0,4\left(g\right)\)
\(V_{CH4}=0,4.22,4=8,96\left(l\right)\)
4.
\(M_{Al2\left(SO4\right)3}=342\)
5.
Gọi công thức A là FexOy
Ta có \(x+y=7\)
Lại có \(M_A=232\)
\(\rightarrow56x+16y=232\)
\(\rightarrow\left\{{}\begin{matrix}x=3\\y=4\end{matrix}\right.\)
Vậy A là Fe3O4