Câu 2 :
a , Trình bày 5 phương trình phản ứng có thể tạo HCl trực tiếp từ Cl2
b , Bằng các PTPƯ hãy chứng minh axit clohidric có thể tham gia các phản ứng và vai trò là :
- Chất khử
- Chất oxi hóa
- Chất trao đổi ( trong phản ứng trao đổi
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$a\bigg)$
$Cl_2+H_2O\leftrightharpoons HCl+HClO$
$CH_4+Cl_2\xrightarrow{ánh\, sáng}CH_3Cl+HCl$
$CH_3Cl+Cl_2\xrightarrow{ánh\, sáng}CH_2Cl_2+HCl$
$CH_2Cl_2+Cl_2\xrightarrow{ánh\, sáng}CHCl_3+HCl$
$CHCl_3+Cl_2\xrightarrow{ánh\, sáng}CCl_4+HCl$
$b\bigg)$
- Chất khử:
$2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2+8H_2O$
- Chất oxi hóa:
$Fe+2HCl\to FeCl_2+H_2$
- Chất trao đổi:
$AgNO_3+HCl\to AgCl\downarrow+NaNO_3$

HCl 2 HCl + Fe → FeCl 2 + H 2 4 HCl + MnO 2 → MnCl 2 + Cl 2 + 2 H 2 O

PT:
Fe + S-->FeS (to)
FeS + H2SO4-->H2S + FeSO4
Vai trò:chất oxi hóa

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
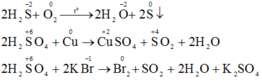

SO 2 2 SO 2 + 2 H 2 O + O 2 → 2 H 2 SO 4 2 H 2 S + SO 2 → 2 H 2 O + 3 S

Cu Br 2
Cu Br 2 là chất oxi hóa
Cu Br 2 + Fe → Fe Br 2 + Cu
Cu Br 2 là chất khử
Cu Br 2 + Cl 2 → Cu Cl 2 + Br 2

a)H2S chỉ thể hiện tính khử vì số oxi hóa của S ở mức thấp nhất :-2 .(Không thể giảm nên chỉ có tình khử)
H2SO4 chỉ thể hiện tính oxi hóa vì số oxi hóa của S ở mức cao nhất :6 . (Không thể tăng nên chỉ có tính oxi hóa)
b)H2S + Pb(NO3)2-->PbS + 2HNO3
H2SO4+ FeS -->H2S + FeSO4

a) KClO3 + 6HCl --> KCl + 3Cl2 + 3H2O
Chất khử: HCl, chất oxh: KClO3
| QT khử | Cl+5 + 6e --> Cl-1 | x1 |
| QT oxh | 2Cl-1 - 2e --> Cl20 | x3 |
b) 2KMnO4 --to--> K2MnO4 + MnO2 + O2
Chất khử: KMnO4, chất oxh: KMnO4
| QT khử | 2Mn+7 + 4e --> Mn+6 + Mn+4 | x1 |
| QT oxh | 2O-2 - 4e --> O20 | x1 |
\(a.QToxh:2\overset{-1}{Cl}\rightarrow Cl_2+2e|\times5\\QTkhử:2\overset{+5}{Cl}+10e\rightarrow \overset{0}{Cl_2}|\times1\)
HCl là chất oxi hóa, KClO3 là chất khử
\(KClO_3+6HCl_{đặc}\rightarrow KCl+3Cl_2+3H_2O\)
\(b.QToxh:2\overset{-2}{O}\rightarrow\overset{0}{O_2}+4e|\times1\\ QTkhử:2\overset{+7}{Mn}+4e\rightarrow\overset{+6}{Mn}+\overset{+4}{Mn}|\times1\)
KMnO4 vừa là chất khử, vừa là chất oxi hóa
\(2KMnO_4-^{t^o}\rightarrow K_2MnO_4+MnO_2+O_2\)